|
Sorafenib治疗肝癌的Ⅲ期临床试验的Oriental研究是对晚期肝癌患者以2:1的比例随机接受索拉非尼单药治疗或安慰剂治疗,以探讨索拉非尼对亚洲人群肝癌治疗的安全性和其生存期改善的情况 。
Oriental研究获得了与SHARP研究基本一致的结果,索拉非尼组患者的生存期(OS)延长了近1倍,表明索拉非尼同样可以显著延长亚洲HCC患者的OS及TT(R)P,从而进一步印证了SHARP研究结果。
SHARP和Oriental研究的比较显示在这两项研究中.晚期肝癌患者被定义为不符合外科手术治疗标准或局部治疗后病情恶化的患者。 SHARP研究纳入欧美人群,以丙型肝炎病毒(HCV)感染引起的肝癌为主,而Oriental研究是在亚太地区开展,以乙型肝炎病毒(HBV)感染的晚期HCC患者为研究对象,虽然Oriental研究中患者的病情分期相比SHARP研究更晚,但两项研究结果却高度一致。这表明,不同种族、地域的HCC患者接受索拉非尼治疗均有显著的临床收益。
索拉非尼与TACE联合治疗的原理 那么能否将索拉非尼与TACE联合起来治疗B期(中期)肝癌,实现索拉非尼在巴塞罗那分期表中应用的左移? TACE联合索拉菲尼的原理 索拉非尼可以显著改善晚期肝癌的生存率[11],而TACE可以改善中期肝癌生存率[12]。两者结合的结果如何呢?所以需要寻找两者间协同作用的证据[13,14]。
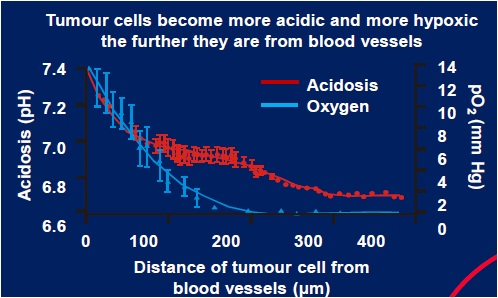
此图所示为:索拉非尼所为络氨酸激酶抑制剂(tyrosine kinase inhibitor)主要靶向目标是细胞内,而DEB-TACE所为细胞毒性治疗其主要靶向目标为细胞的复制(targets cell replication)。 TACE术后肿瘤内及其周围最大的微环境变化是缺氧。而缺氧导致血管的发生(下图)[3]。VEGF是肿瘤新生血管(生长和通透)关键介质。
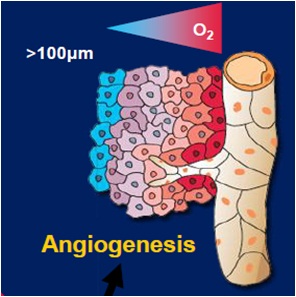
缺氧导致血管发生(Angiogenesis)
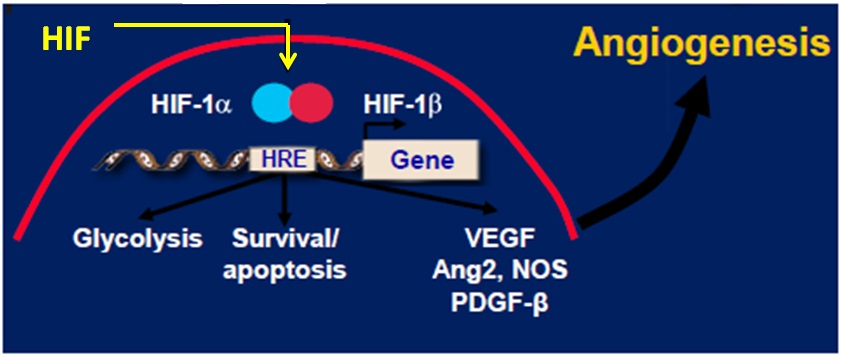
HIF = hypoxia inducible factor; HRE = hypoxia response element; Ang-2 = angiopoietin-2; NOS = nitric oxide synthase; PDGF-β = platelet-derived growth factor-β
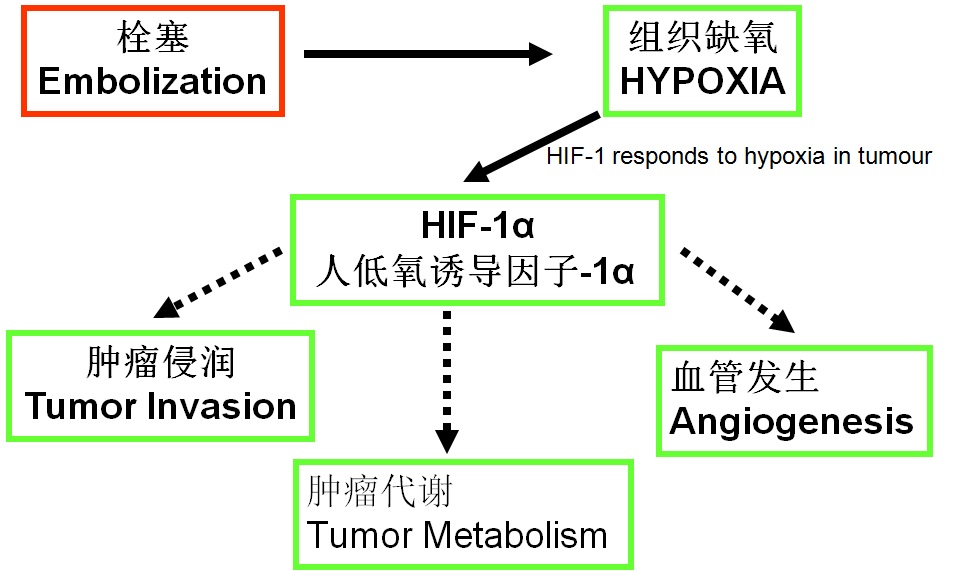 栓塞后缺血的肿瘤及周围的间质细胞会分泌促血管生成因子(VEGF)刺激血管的发生。这一过程使栓塞后的肿瘤向多血管肿瘤演变,导致肿瘤的快速生长以及侵犯和转移。而血管发生抑制因子可以防止多血管化并使血管发生退行性变使肿瘤缺血[5]。VEGF是血管发生的中心介质(下图)[6~8]。 上图所示很多因素可以导致VEGF的发生,其中TACE可以导致肿瘤微环境的改变,缺氧和pH的升高刺激VEGF的发生,VEGF与细胞受体的绑定内皮细胞激活使血管发生细胞发生增殖,迁徙以及存活。
尽管肝癌的TACE可以使肿瘤缺血,使肿瘤缩小。但栓塞导致的VEGF升高使肿瘤复发。所以将TACE与抗血管生成药物联合治疗肝癌成为理所当然的事,结果如何呢?
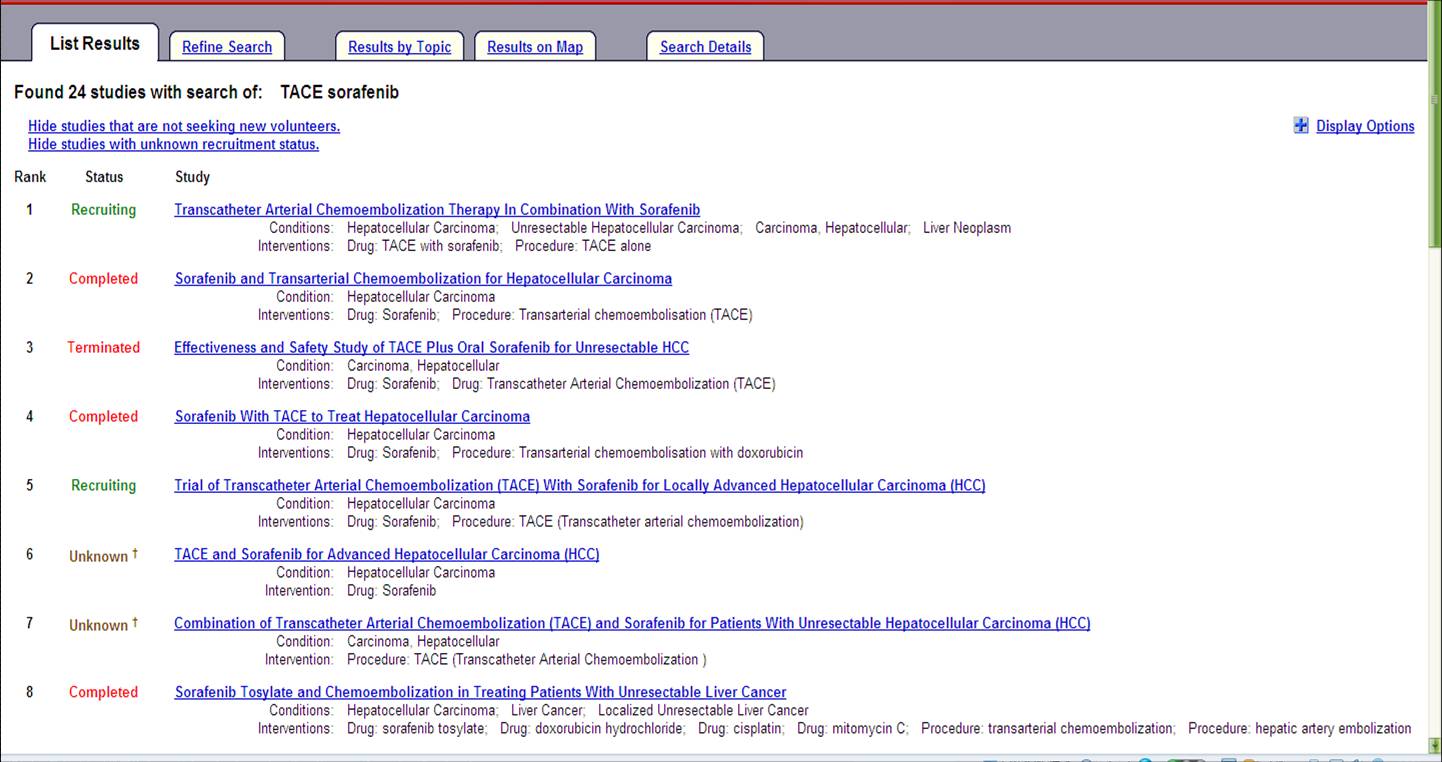
TACE+抗血管生成药物治疗HCC在www.clinicaltrial.gov 注册N多项的研究。包括Bevacizumab 4项,Brivanib 1项,Thalidomide 4项,Sunitinib2项,Everolimus 2项,TAC101 1项,Axinitinib 1项。作为分子靶向药物Sorafenib有24项。其中有些使用常规TACE,有些则应用DEB-TACE。实验包括I,II 和III的研究,研究终点包括TTP,PFS,TTUP等,这些研究都是希望可以在临床证实分子靶向药物与TACE联合可以提高治疗的效果。
SPACE: 随机对照,TACE + 索拉非尼(www.clinicaltrials.gov/ct2/show/NCT00855218)
ECOG III trial TACE+索拉非尼(www.clinicaltrials.gov/ct2/show/NCT00855218)
ECOG Eastern Cooperative Oncology Group (one of the largest clinical cancer research organizations in the United States )
不可切除肝癌 II Trial:DEB- TACE+ 索拉非尼(Johns Hopkins University )
1. Llovet et al. J Natl Cancer Inst 2008;100:698
2. Hanahan D and Weinberg RA. Cell 2000 4. Wilhelm SM et al. Cancer Res. 2004:64 7099-7109 5. Carmeliet & Jain Nature 2000; 407:249.
6. Dvorak. J Clin Oncol 2002;20:4368. 9. Sergio et al. Am J Gastroenterol 2008;103:914. 10. Li X, et al. W J Gastroenterol 2004;10:2878–82
11. Llovet et al, N Engl J Med, 2008;359:378-90 14. Richley,et al, Ann Oncol, 2006. 15. Spangenberg HC, Thimme R, Blum H: Targeted therapy for hepatocellular carcinoma. Nat Rev Gastroenterol Hepatol 2009;6:423–432. 16. Thorgeirsson S, et al. Hepatology. 2006;43:S145-150. 17. Avila MA, et al. Oncogene. 2006;25:3866-3884. 18. Abou-Alfa GK, et al. J Clin Oncol. 2006;24:4293-4300. |