肝癌是2020年全球第六大常见癌症和第三大癌症相关死亡原因,约有906,000例病例和约830,000例死亡【Sung H, 2020 】。经动脉化疗栓塞(TACE)是世界范围内肝细胞癌(HCC)最常用的治疗方法之一。肝细胞癌(HCC)约占原发性肝癌的90%,是肝硬化患者死亡的主要原因【Fattovich G, 2004 Ioannou GN, 2007】。在大多数地理区域,HCC的年死亡率几乎与其发病率相当。证实了该肿瘤的高死亡率 [美国的5年生存率为12%-14%,意大利为20% ]【Mittal S, 2013 意大利肿瘤注册协会】。尽管努力促进筛查的计划,以使早期肝癌诊断并增加,提高患者可治愈性治疗的百分比【Trevisani F, 2002 Pelizzaro F, 2021 Pelizzaro F,2021】,但HCC经常在晚期才被发现,因此多数肝癌患者被排除了提供根治性治疗的可能性,如肝移植(LT),肝切除(LR)或消融(ABL)【Galle PR, 2018】。
根据巴塞罗那临床肝癌(BCLC)算法,经动脉化疗栓塞(TACE)是中期HCC患者的标准治疗方法【Galle PR, 2018】。然而,它也被广泛应用于BCLC B期以外,例如C期,甚至A期。这使得TACE成为全球日常临床实践中最常用的HCC治疗方法之一【Park JW, 2015 Bargellini I, 2014】。考虑到较低完全缓解率和较高疾病复发率,TACE根据定义是一种姑息性和需要反复治疗的手段【Lo C-M, 2002 Lammer J, 2010 Golfieri R,2014】。
没有明确的证据表明,无论肿瘤反应如何,按时 (例如每1-2个月)安排TACE(scheduled TACE),对患者生存的影响不同于按需进行TACE(On demand TACE)。然而,采用积极的治疗方案可能会导致很大比例的患者发生肝功能衰竭,其中大多数患者还伴有肝硬化。因此,根据指南的建议,只有在影像发现到残留的活肿瘤时才进行TACE治疗(按需TACE),这种按时TACE的方法已经基本放弃了。 当两次后续尝试均未获得显著的肿瘤反应时停止TACE治疗【Galle PR, 2018】。然而,在临床实践中,TACE治疗经常重复多次,特别是在部分反应或首次治疗成功后复发的患者中。然而,反复TACE的益处是不确定的,也因为这些患者的生存预测是一个困难的问题,只有复杂的重新校准(recalibration)【Cucchetti A, 2021】或时变模型(time-varying model)(即mHAP-III)【Campani C, 2021】似乎才能准确解决。由于基于酪氨酸激酶抑制剂、雷莫芦单抗(ramucirumab)和免疫疗法的几种有效全身疗法的可用性不断增加,这种不确定性增加了【Llovet JM, 2008 Kudo M,2018 Bruix J, 2017 Abou-Alfa GK, 2018 Zhu AX,2019 Finn RS, 2020】。事实上,全身治疗可能是一种有效的(可能更好的)替代TACE。为了支持患者的重复TACE决策,已经提出了ART评分【Sieghart W, 2013 Hucke F, 2014】和ABCR评分【Adhoute X, 2015】等几种算法。
尽管TACE经常被用于治疗HCC,但很少有研究调查其使用是否随着时间的推移而改变。此外,很少有证据表明,在现实的临床实践中,接受TACE治疗的患者的百分比,随着时间的推移,这一百分比的变化趋势,以及与其他治疗方案相比,接受经动脉治疗的患者的结果。Pelizzaro F 等人考虑到意大利肝癌(ITA.LI.CA)数据库中30年的大量患者的可用性,评估在现实临床实践中TACE的使用及其结果是否随着时间的推移而改变,以及指导这种治疗选择的肿瘤学和临床特征。此外,评估了重复TACE的时间趋势和接受反复治疗的患者的结果【Pelizzaro F, 2022】。
TACE治疗过程中:重复TACE的频率和时间究竟是多少? 肝癌的治疗都已经进入到靶免治疗的时代,历经20多年,理想的TACE策略还远没有一个清晰的定义。除了肝癌治疗的医学进步使然,还一个就是肝癌是一个异质性疾病。 每一项技术都会面临诸多的临床情形,包括肝癌的宿主变量,肿瘤本身变量和治疗技术变量。多年来各种经动脉导管技术不断被深化,但没有哪一项技术是优效性的,包括TACE vs TAE。减少每一项动脉导管技术的危害性就成为另一种重要的考虑因素。 重复TACE是肝癌经导管化疗性栓塞常见的操作,指为了追求潜在肿瘤完全坏死需要反复进行TACE,并潜在提高患者的生存率【White JA 2014】。反复TACE通常被分为按时TACE和按需TACE。
按时TACE
间隔固定时间给予患者预定次数的 TACE【Lu J 2021】的按时TACE或Scheduled TACE。但既往肿瘤化疗原理出发,按照细胞分裂周期,无论前次 TACE 后的肿瘤反应如何【Zhong BY 2023】,即使肝内肿瘤反应良好,也以固定的时间间隔进行重复 TACE,有时不必要的TACE可导致导致肝功能受损,虽然基于细胞周期的标准化疗疗程预定策略更符合肿瘤化学治疗的一般原则。但按时TACE的理念已经过时,这一页已经翻过去了。 按需TACE
按需TACE,又称为on-demand TACE。是根据 TACE 后的肿瘤反应、肝功能以及患者状态判断是否再次进行 TACE。这是基于TACE治疗肝癌是以姑息性治疗为目的的。已经达到部分缓解或者稳定的情况下无需按固定的时间间隔重复TACE。重复TACE的最小间隔时间或最长间隔时间,或究竟每年可以重复TACE几次都没有最佳策略的证据。但无论如何,需要避免重复TACE可能诱发肝功能衰竭。要关注患者重复TACE治疗后的状态【中国TACE指南2023】
早先没有靶免全身治疗的时代,患者在初次TACE治疗后有残留的重要肿瘤和PR(或至少SD)。我们不断重复TACE,即使是TACE抵抗后,包括TACE后主病灶复发、出现新发病灶,甚至出现肝外病变,我们依然对治疗抱有希望,当时无标准化的再治疗政策【Kloeckner R 2020】。关于最佳的再治疗方案,也无明确证据表明,在预定的时间间隔后重复TACE或在疾病进展时重复TACE是否更好。继续TACE治疗,直至因肝功能衰竭而终止治疗。当时所谓的全身治疗只是最好的支持治疗,或安慰治疗,和缓医疗或中医治疗。 已经更新的观点认为遇到TACE抵抗时,尽快使用全身治疗。甚至不等TACE开始,肝癌的一线治疗初始就从全身治疗开始,哪TACE咋办?或许按需TACE这一页历史也翻篇儿啦,或者重新定义 根据最初试验的积极经验,通常的做法是在1 ~ 2个月内进行两次TACE初始治疗,因为这可能会获得更好的缓解率【Georgiades C 2012】。之后,定期间隔对病例的监测,可能会改善TACE的结果。但积极的计划也可能增加肝衰竭的风险【Georgiades C 2012;Kim SO 1995】。无论哪种方式,都必须密切监测肝功能和体力状态,以避免“过度治疗”【Miksad RA 2019】。 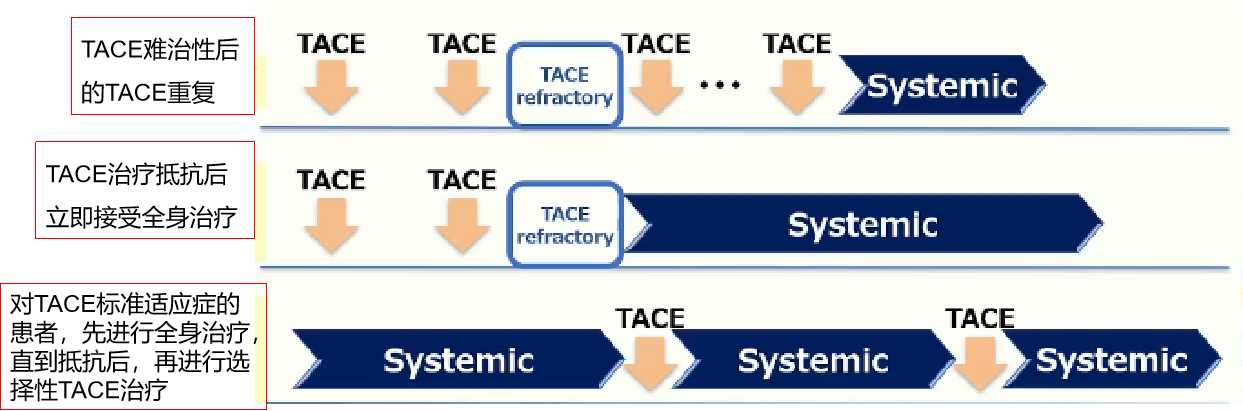 靶免时代,由多学科肿瘤委员会(包括经验丰富的肝胆外科医师、肝病医师、介入放射科医师和肿瘤科医师)对每例患者进行TACE后持续重新评估至关重要,在后续治疗仍有可能的情况下,不要错过转换为全身性靶免治疗的最佳时机,更不要错过达到降期标准肝切除或肝移植的机会。 因此,在每次TACE治疗前,疗效评估是必不可少的。为此,应在TACE前立即进行影像学检查(CT/MRI)。这样,除了疗效评估之外,还可以记录上述代表肿瘤生物学的重要因素,如甲胎蛋白等。 在cTACE中,CT图像上碘油蓄积的程度与肿瘤坏死的程度相关【Dioguardi 2019;Takayasu K 2000】。然而,由于CT中碘油染色的“盛开效应(blooming effect)-碘油可能掩盖代表肿瘤复发的新的CT增强部分”,改用MRI可能有助于评估残留的存活肿瘤组织【Kloeckner R 2010】。DEB-TACE后,CT和MRI可以互换使用【Kloeckner R 2010】。
初次TACE成功并获得CR后,复发可表现为治疗肿瘤的再血管化【Galle PR 2018】,也可表现为新的肿瘤病灶。对于这两种情况,重复TACE可能是确保治疗成功的必要条件。然而,为了确保特定的患者仍然是良好的TACE候选人,跨学科肿瘤委员会的讨论也是最重要的。 TACE治疗HCC的目的是局部控制或缩小肿瘤。之前的一些研究表明,重复cTACE可最大限度地提高肿瘤反应并延长OS。重复TACE可能与肝损害和不良反应增加相关。因此,需要在再次TACE的必要性和治疗之间取得微妙的平衡
如果TACE最初无反应或出现“不可治疗的进展” (定义为肝脏大面积受累、肝外播散、血管侵犯、肝功能受损或体力状况恶化),则应立即停止TACE【Kloeckner R 2020;Raoul JL 2014 】。
总结以上,初次TACE后,面对PR/SD,完全缓解或进展的情况,TACE应对是不同的。有必要对每例患者进行重新评估。治疗反应是进一步治疗的一个不可或缺的因素,因为它是中位OS的强预测因素,可以被视为一个荟萃分析时的参数。
由于肿瘤坏死并不一定伴随着肿瘤体积的立即缩小【Kloeckner R 2020】,传统的基于肿瘤最大直径的RECIST标准可能倾向于低估肿瘤的反应。由于HCC主要是动脉(超)血管化,因此已经制定了测量造影增强组织最长直径的改良RECIST (mRECIST)标准,这是西方指南推荐的缓解情况评估方法。与传统标准一样,TACE治疗后患者的缓解可分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)或疾病进展(PD)。以当前形式显示了mRECIST标准的详细描述。
若前次栓塞后,不考虑再次栓塞
综上所述,TACE依然作为作为广泛采用的肝癌治疗手段,重复TACE应根据患者治疗后的状态决定。
按需TACE的考虑更多的是安全性,但两者比较会不会有生存上的获益呢。接受TACE治疗患者的总生存率仍然很低,3年生存率还不到30%。按需TACE(on demand)是不是一种提高生存率的策略呢? 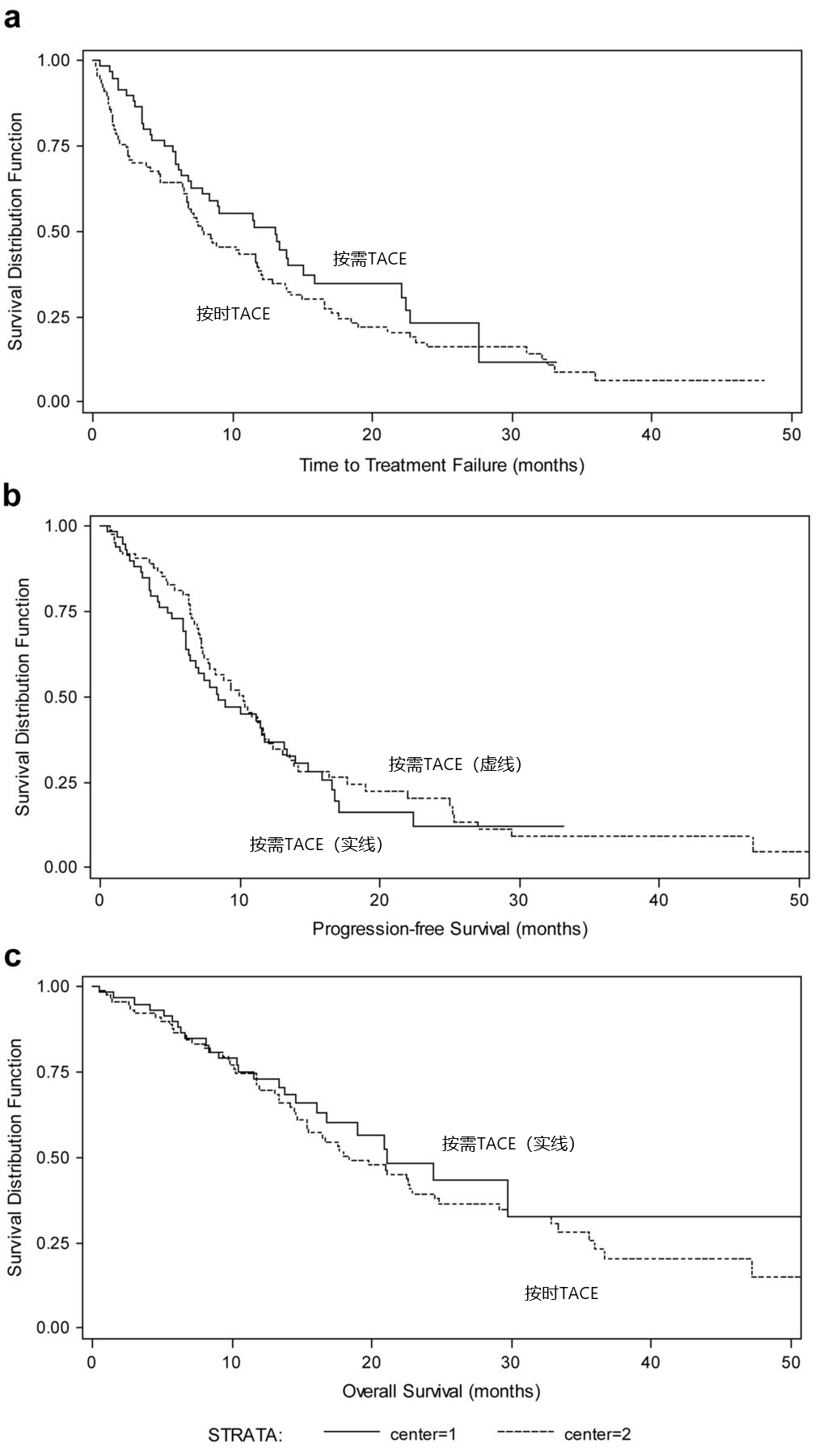 总之,结果表明,在法国两个中心实施的TACE策略之间,PFS或OS没有任何差异。在一个中心观察到的≥3级不良事件患者比例显著较高,这可能解释了该中心总体TACE策略的中位住院时间显著较长。 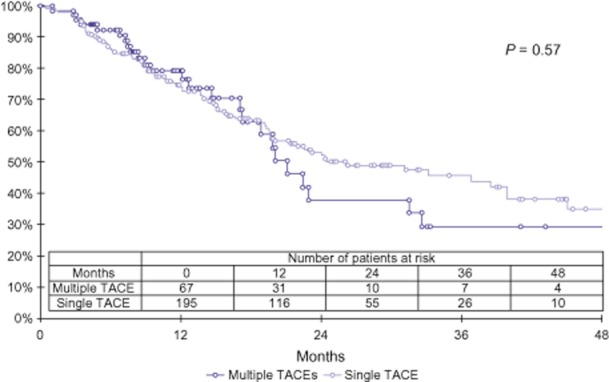 考虑到TACE的姑息性,通常需要再次TACE才能达到更好的肿瘤控制和长期预后。之前的几项研究发现,重复TACE可带来生存获益【Terzi E, 2012】。然而,重复TACE与副作用增加和肝功能受损相关。因此,必须仔细权衡潜在的治疗获益与再次TACE的副作用。目前临床实践中重复TACE治疗的模式主要有预约随访和按需模式。对于按需模式,只有在常规随访期间观察到有存活的肿瘤或局部和/或远处肝内复发时,才考虑重复TACE 【】11值得注意的是,存活肿瘤的概念尚未得到准确定义。对于预定模式,无论上次TACE后肿瘤缓解情况如何,均以固定时间间隔重复TACE。 更令人不解是是重复TACE可能不带来生存获益
根据EASL,如果在两轮治疗后未达到实质性坏死,或者当后续治疗未能在初始肿瘤缓解后发生进展的部位诱导明显坏死,或者如果发生不可治疗的进展(定义为与临床特征相关的肿瘤进展,可防止再次治疗),则不应重复TACE 11值得注意的是,JSH表明肝内新发病变是肝脏疾病的自然过程,不应将其视为疾病进展。因此,如果出现新的肝内病变,则不应停止TACEAASLD和CNLC均未提供关于停止TACE的最佳时间的详细建议7,12。已有几种预后模型或评分被用于帮助对更有可能从初次或再次TACE中获益的患者进行分层。然而,这些模型均未被指南强烈推荐42,43
TACE失败/难治性的概念是为了避免无效的重复TACE 44 - 46。临床实践和临床试验中应用最广泛的是日本jsh -肝癌研究组(LCSGJ)的定义,并于2014年进行了更新44然而,这种定义的客观性和合理性仍存在争议。在无高级别证据支持的情况下,该概念建议在发生TACE失败/难治性的情况下转为全身单药治疗。相比之下,最近发表的一篇文章综述了TACE失败/难治性后后续治疗的现有证据,得出结论认为,不仅索拉非尼,其他疗法(如TACE联合药物洗脱珠、肝动脉灌注化疗、消融和TACE联合全身性治疗)也有可能作为TACE失败/难治性后的后续治疗47此外,2020年中国介入医师学会(CCI)在全国范围内开展的一项网络调查发现,基于现有的TACE失败/难治定义,中国临床医师对TACE失败/难治的认知存在明显差异最近,CCI发布了肝癌TACE难治性及后续治疗的专家共识49。CCI对TACE难治性的定义是在连续3次或以上的标准化和精准TACE治疗后,与基线相比,所治疗肿瘤发生进展(根据mRECIST标准,在最近一次TACE后1 ~ 3个月,增强CT/MRI显示疾病进展)。
|







