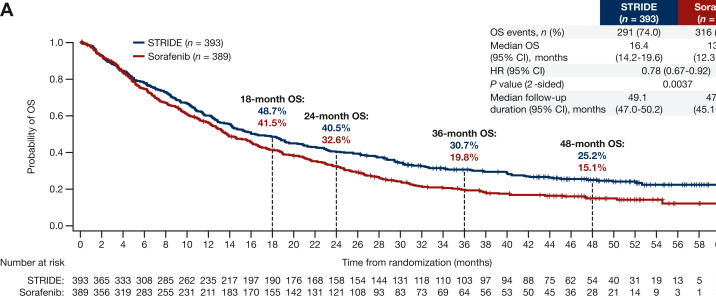
| 肝癌新药,FDA批准双免疫治疗方案STRIDE用于治疗肝细胞癌 双免疫治疗方案:首个获批用于肝癌一线的双免疫联合疗法,被称为STRID方案(HIMALAYA) PD-L1 德瓦鲁单抗(durvalumab)+ CTLA-A 曲美木单抗(tremelimumab) 在针对不可切除的肝细胞癌 (uHCC) 的 III 期 HIMALAYA 研究 (NCT03298451) 中,STRIDE(单次 Tremelimumab 定期间隔 Durvalumab)与索拉非尼相比显着改善了总生存期 (OS);在 OS 方面,durvalumab(杜伐尤利单抗) 单药治疗并不劣于索拉非尼。本文报告的结果来自 HIMALAYA 的 4 年更新 OS 分析。 亮点 • uHCC III 期 HIMALAYA 研究的最新分析显示,与索拉非尼相比,STRIDE 具有持续的 OS 优势。 • STRIDE 组的四年 OS 率为 25.2%,索拉非尼组为 15.1%。 • 与索拉非尼相比,STRIDE 改善了各亚组的 OS,并进一步改善了疾病控制患者的 3 年和 4 年 OS 率。 • 索拉非尼组与 STRIDE 组相比,随后的抗癌全身治疗更为常见。 • 对STRIDE 进行初步分析后,没有发生新的严重治疗相关AE。 4年更新分析中STRIDE与索拉非尼的OS
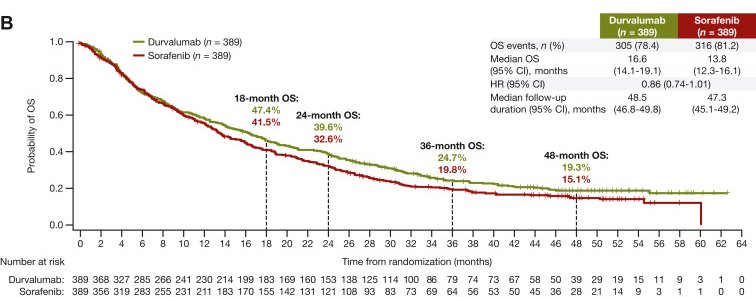
durvalumab(杜伐尤利单抗)与索拉非尼的OS
直到2020年,不可切除HCC (uHCC)的一线治疗仅限于酪氨酸激酶抑制剂索拉非尼和lenvatinib(仑伐替尼)。
在uHCC的随机III期临床研究中,基于免疫检查点抑制剂(ICI)的联合方案,包括
- STRIDE (Single Tremelimumab Regular Interval Durvalumab)、 - atezolizumab(阿替丽珠单抗) +贝伐单抗、 - camrelizumab(卡瑞丽珠单抗) + rivoeranib(阿帕替尼) 这些方案与索拉非尼相比,显著改善了OS。
STRIDE方案已在全球范围内获得批准,作为uHCC的一线治疗方案。Durvalumab单药疗法也已在日本和欧盟被批准用于治疗成人uHCC。
III期HIMALAYA研究 (NCT03298451) 评估了STRIDE方案,双ICI(检查点抑制剂)联合,durvalumab(杜伐尤利单抗)单药治疗与索拉非尼在未接受过全身治疗的uHCC患者中的应用。
STRIDE方案包括在第一个周期使用单剂量的tremelimumab (一种抗细胞毒性t淋巴细胞相关抗原4 (抗ctla -4) 抗体)和durvalumab(杜伐尤利单抗,一种抗程序性细胞死亡配体-1(抗pd - l1)抗体)进行治疗,然后每4周使用durvalumab(杜伐尤利单抗)单药治疗。
HIMALAYA 研究招募了不同人群的参与者,反映了全球uHCC人群,并且在肝脏疾病的病因之间是平衡的。在喜马拉雅的初步分析中,中位随访时间为~ 33个月(数据截止日期:2021年8月27日),STRIDE方案与索拉非尼相比显着改善了OS, OS风险比 (HR)为0.7 8 [96.02%置信区间(CI) 0.65-0.93;P = 0.0035]。
Durvalumab(杜伐尤利单抗单药治疗OS不逊于sorafenib (HR 0.86, 95.67% CI 0.73-1.03,非劣效边际1.08)。
虽然没有正式的测试,但在36个月的OS率上,STRIDE(30.7%)与索拉非尼(20.2%;P = 0.0029)。
STRIDE方案显示出与其他目前可用的uHCC治疗相比具有可耐受和差异化的安全性。
STRIDE和durvalumab(杜伐尤利单抗)不良事件(ae)的发生率、频率和严重程度与每种药物已知的安全性一致,STRIDE和durvalumab单药治疗相关ae的频率低于索拉非尼。
此外,大多数使用STRIDE 或 durvalumab杜伐尤利单抗 的免疫介导ae是在治疗开始后的前3个月内观察到的。
这项为期4年的喜马拉雅研究随访分析报告了STRIDE方案和durvalumab(杜伐尤利单抗)单药治疗与索拉非尼的OS和安全性,包括长期幸存者的特征。这是迄今为止在肝癌关键III期研究中最长的随访。
|