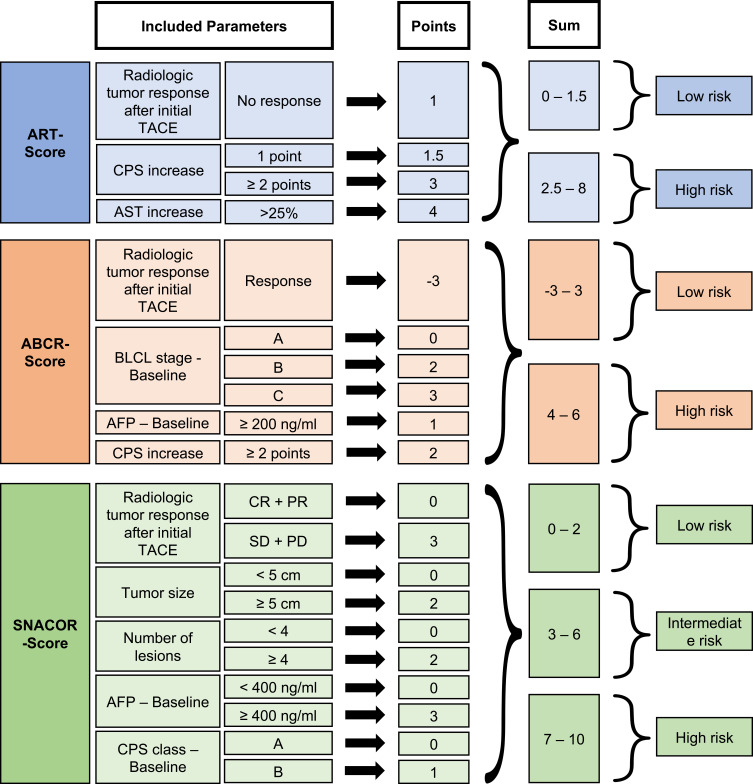
������������TACE��ʼʱ��TACE��ǰ���֣��Ľ�����ƣ��������ڼ���TACE������ϵͳ��TACE�������֣���δ��ͨ���������ⲿ��֤���ڸ���Ԥ��Ԥ�ⷽ��������е�ȷ�ԡ�������Lukas Muller ʹ���Լ������ݶ�ART��ABCR���ֽ�����֤��������������ϵͳ���ܹ����ݻ��ߵ���λOS�Ի��߽��зֲ㡾Kloeckner R 2017���������仼�߶��У�ABCR������ȷ��Ȼ�������������ڸ���Ԥ��Ԥ�ⷽ��ļ�ֵ��Ϊ�еȡ����⣬Lukas ������SNACOR���֣�������Ҳ������������λOS�Ի��߽��������ֲ㣬���ڸ���Ԥ��Ԥ�ⷽ��ʧ�ܡ�Mähringer-Kunz A 2018����
����������Щ�൱����ʧ���Ľ����EASLָ��ר������Ϊ����ϵͳ��ʹ�ô������飬�����鵱�������ƺ�δ�ﵽʵ���Ի������������δ���ڳ�ʼ����������չ�IJ�λ�յ����Ի���ʱ����Ӧ�ظ�TACE��Galle PR, 2018����
���ߵõ���Georgiades���˵�֧�֣����ǵ��о��������ھ����Ƿ����TACE֮ǰ�����������������TACE������Georgiades C 2012��
��֮�������������־�������Ԥ������֧����ȷ���ٴ����ߡ���ˣ���Ϊһ���ɾ���ḻ�ĸε����ҽʦ���β���ҽʦ����������ҽʦ��������ҽʦ��ɵĿ�ѧ������ίԱ�ᣬ�б�Ҫ����ÿ��TACE���Ƶ���Ӧ֤���ر��ǣ����뿼�Ǹ��������ķ�Χ���ι��ܺͻ��ߵ�����״̬������ߵ����Ӧ��Ϊ���߹����в��ɷָ��һ���֡��ر���TACE���Ƶ�������Ԥ���Ӱ��Ӧ�ھ����з�����Ҫ���á�
��ǰ������ϵͳ:Ϊʲô����������ʧ��/���ֲ���?
����ϵͳ����֤������˾�ɥ��һ�����ܵ�ԭ������Ǿ������HCC���ߺϲ���Ӳ������ʹԤ���ø��ӡ�����һЩ������ͼ�������������棬����ʹ��3 ~ 5�����������ǶԸ�Ϊ���ӵ��ٴ���ʵ�IJ��ʵ���
֮ǰ����������ϵͳ���ǻ��ڻ�������ͬ����ѧԭ��������: ������ع����������������ϵ�������ǻ��ھ�������ѡ��Ķ��е����ݼ����е����ļ�Ȩ���ӡ���ˣ�����Ͽ�������÷�����ص�һ������ѧ���⡣�������������“��һ��ģ����ijЩ���ݼ��ϵ�������������ڲ�ͬ�ٴ����˿�ͳ��ѧ�����»��������������������Ԥ���������������ط��õ�֤ʵʱ���ֵ�һ������”��Facciorusso A 2015����������������ڵ�һ���������ģ�����ܼӾ��˹�����ϵ����⡣���⣬������о��������е���������
�����˹����ܵ��·���
Ϊ�˿˷���Щ�����ԣ��ڸΰ����ߵ�TACE������ʹ���˹�����(AI)�����˼��γ��ԡ�Abajian A 2018��
Peng J 2020��
Mahringer Kunz 2020��
Liu D 2020������Щ���Կɷ�Ϊ���顣Peng���ˣ�ababjian���ˣ�Liu����רע��ѵ�������˹����ܵ�ϵͳ����ϵͳ�����ڵ�һ������ǰ����TACE���Ƶķ�Ӧ��Peng����ʹ��CTͼ�����ģʽʶ��Peng J 2020���÷�����ѵ������֤�о��������õ�ȷ�ԡ�Ϊ������TACE���������Ӧ��abajan�Ȼ�������������MRI�����������ٴ�����������һ��ģ�͡�Peng J 2020������Ȼ���ǵ�ϵͳ��ȷ���Եͣ�����γ���ǿ���˻����˹����ܵĽ�������������������Liu��֤����ʹ�ó�����Ӱ��Ӱ��������Ԥ��Ļ������ѧϰ��Ӱ����ѧģ�͵Ŀ����ԡ�Liu D 2020��Mähringer-Kunz���������������һ�����˷����Ľ��:Ŀ����ѵ��һ������ai��������Ԥ��1�������ʡ�Mahringer Kunz 2020����Ϊ�����Ԥ���ȷ�ԣ�����������46���������������������������������С��������������������ģʽ�����������ι��ܵIJ�����HCC��չ��Σ�����أ��Լ��µ����Ͳ������������ָ�������ǵ��·�����ѵ������֤������ȡ�������õĽ����ROC����������ֱ�Ϊ0.77��0.83����Ԥ��1�������ʷ��棬�÷�����Ч������ART��ABCR��SNACOR���֡�
������Щ�����˹����ܵ�ϵͳ�ĺô������ǵĶ�̬ѧϰ����;�������Բ�ͬ�����ĸ�����ú����������ݼ�����Щϵͳ��ȷ�Կ��ܻ��һ����ߡ�Ȼ���������ϵͳ�������ⲿ��������������֤����ȷ�ԡ����⣬�����еķֲ�ϵͳ��ȣ��ٴ������еĶ�������ж�����д�̽�֡�
