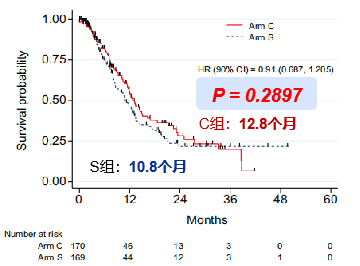
临床研究显示,TACE联合索拉非尼较单一TACE应用比较,均告失败
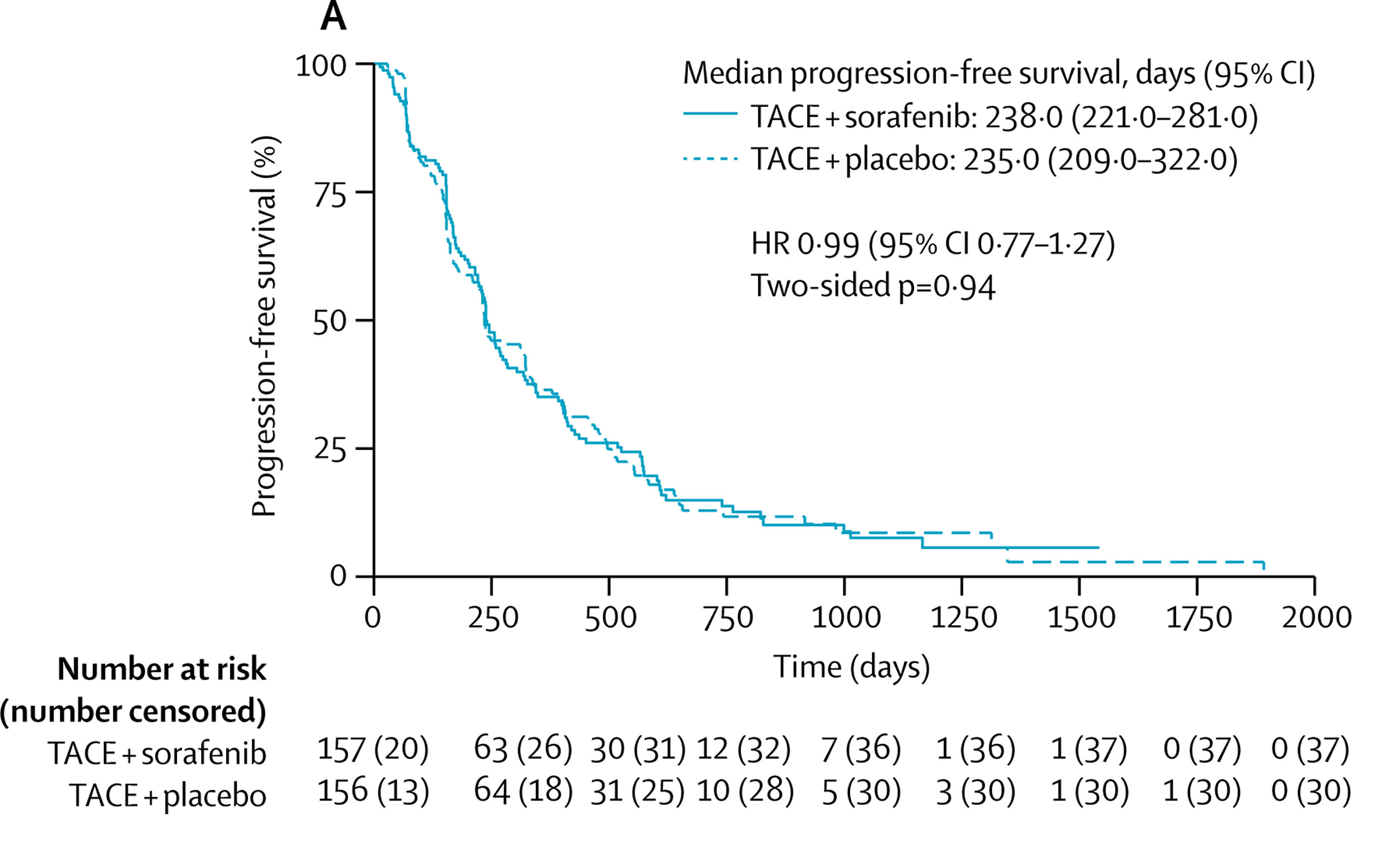
TACTICS II 研究【Kudo M 2022】:随机、开放标签、多中心研究,纳入不可切除患者156例,旨在比较TACE联合索拉非尼与单纯 TACE 的疗效和安全性,主要终点为PFS与OS 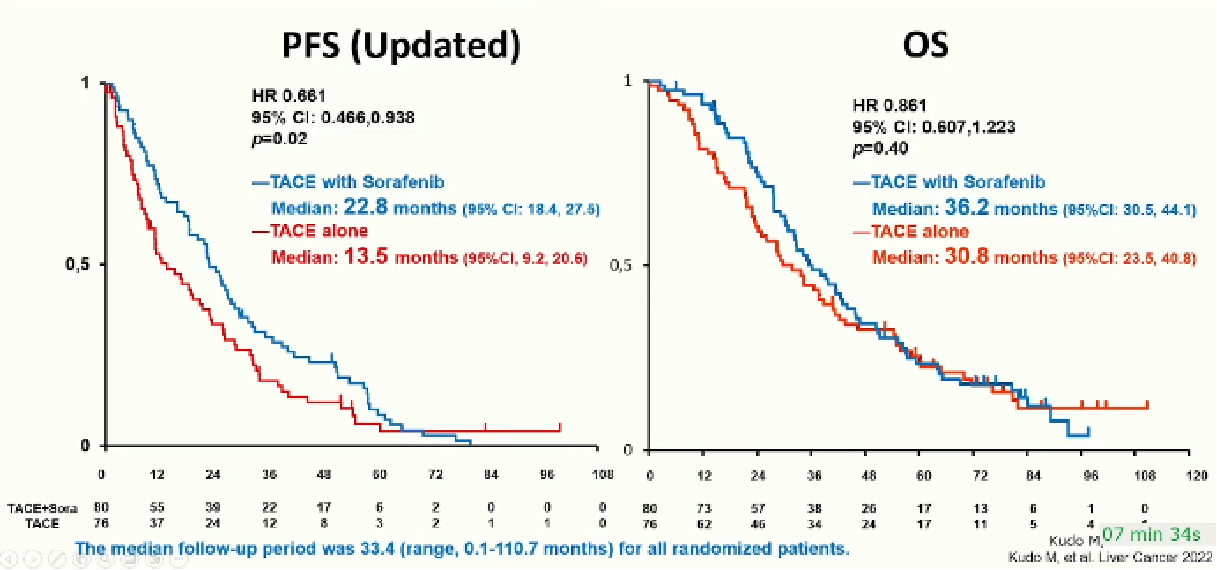
尽管TACE 联合索拉非尼与单一TACE 的PFS 为22.8 个月 vs 13.5 个月,P=0.02,OS 分别为36.2 个月 vs 30.8 个月,P=0.40
TACE 联合索拉非尼较单一TACE明显改善不可手术切除 BCLC A/B 期肝癌患者的 OS 差异无统计学意义。
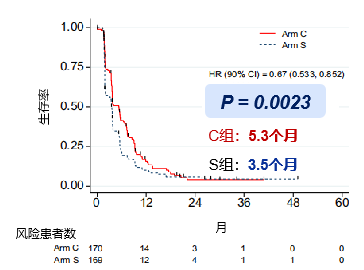
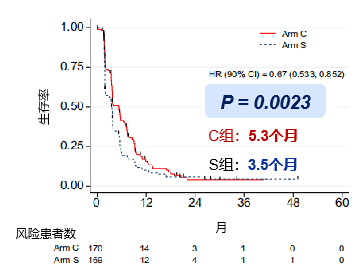
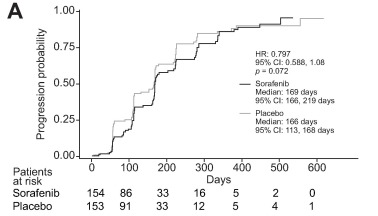
在这之后,Kudo 等人开始了TACTICS-L的研究,试图证明TACE+仑伐替尼 > 单一TACE STAH:TACE+索拉非尼治疗晚期肝癌,虽然显著改善TTP,PFS
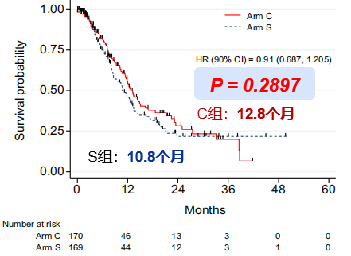
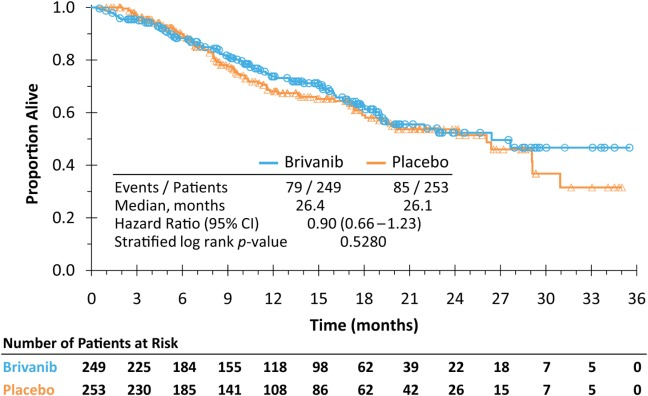
对于 BCLC C 期的HCC患者,TACE 联合索拉非尼较单一索拉非尼无生存获益(12.8 个月 vs 10.8 个月;P= 0.29)
肝癌是一个异质性疾病,对肝癌的治疗需要细分 或许对于中负荷和肝功能ALB1 1分的肝癌患者,TACE联合索拉非尼可改善患者的OS和PFS【Wang Zhexuan 2020】 一项中国三级医院进行,多中心回顾性观察性研究,纳入接受 TACE 或 TACE-索拉非尼治疗的不可切除、局限于肝脏的HCC患者,评价治疗与基线变量的交互作用,寻找生存获益的指标,据此对患者进行分层;旨在确定TACE联合索拉非尼生存获益的预测因素,并确定TACE-索拉非尼的潜在候选者。 只是当时仑伐替尼作为肝癌适应症已经获批(2018年),鲜少有人还重视。2020年以后索拉非尼和索拉非尼与TACE的联合治疗,特别是仑伐替尼,更有阿替利珠单抗+贝伐单抗(T+A)压倒性优于索拉非尼和索拉非尼联合治疗,后续索拉非尼这类文章的发表多由于启动的时间早....,这类文章也鲜少被引用。 TACE+分子靶向药物 III期临床试验 主要终点 OS 或PFS
事实上,TACE仍然是中期HCC的标准治疗,目前广泛用于不适合经皮消融的早期肿瘤。TACE可提高生存率,因为它可以延缓肿瘤进展,有时通过广泛坏死后的完全缓解,治疗反应是TACE术后生存的独立预测因素【Fillmore R 2011】。 TACE的性能和安全性基于结节数量、大小和形态、放射科医生的专业知识和肝功能。使用药物洗脱珠(TACE- deb)进行化疗栓塞,除了可导致更持久的药物释放,同时可以进行栓塞,虽然它简化和协调了TACE方式,但性能与碘化油的传统TACE (cace)大致相似【Golfieri R 2014】。 尽管在患者选择、TACE方式、疗效 [使用修订的实体瘤反应评估标准(mRECIST) ]和停药标准方面有了重大改进【Raoul J 2011】,这种治疗通常不能实现对疾病的持续控制,尽管在大约50%的患者中有客观反应【Lencioni R 2016】。局部和/或远处肝内复发通常被观察到,包括在TACE后获得完全缓解的患者【Labeur TA 2019】(肝癌患者TACE后生存的影响不能持续),即使是在侵袭性更强的肿瘤边缘不光滑的模式【Adhoute X 2017】下,最后是TACE耐药。 原因有很多: 手术过程缺乏安全界限,包膜肿瘤侵袭,微卫星病变【Kuroda C 1991】,早期HCC中分化良好的肿瘤部分(8)通常都由肝动脉和门静脉供血【Tajima T 2002】。此外,反复TACE后动脉血流受损导致的HCC结节门静脉供应可能有助于肿瘤存活【Miyayama S 2011】。新生血管生成是对缺氧的既定反应,TACE诱导的缺氧刺激残留肿瘤细胞产生血管内皮生长因子(VEGF)【Li X 2004】,增加肿瘤血管生成和侧支循环的形成,导致TACE失败。因此,抗血管生成治疗可以提高TACE的疗效【Jiang H 2007】。TACE联合索拉非尼(sorafenib)是一种多激酶抑制剂,靶向抗血管生成因子VEGFR2和PDGFR。因此,TACE联合索拉非尼在2期和3期研究中进行了探索,在疗效方面结果不佳(上表)。 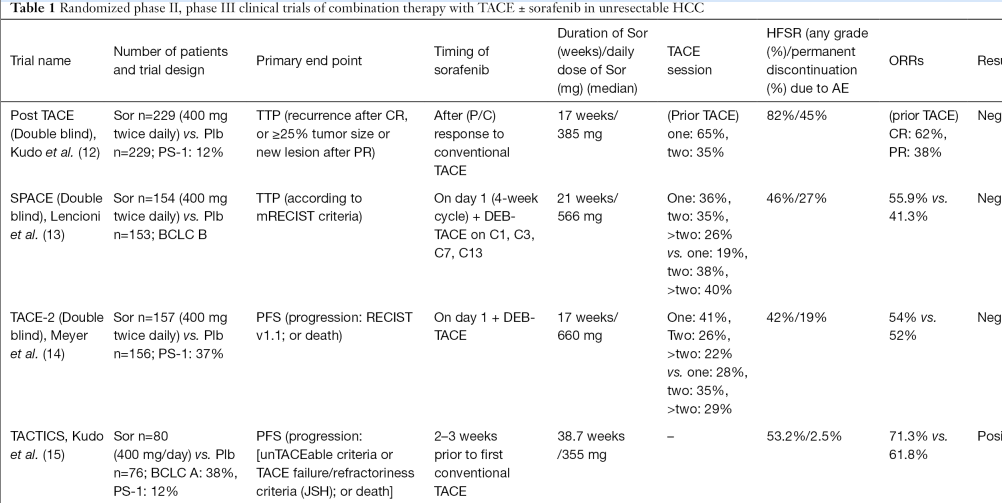 然而,研究设计【Kudo M 2011】、疗程【Lencioni R 2016】或入组人群受到了挑战。在一项新的前瞻性随机对照研究中,Kudo等人报道,基于不可切除HCC患者进展的新定义,cTACE联合索拉非尼可改善无进展生存期(PFS)【Kudo M 2020】。该研究纳入了体力状态略有改变的HCC患者(PS-1),就像评估这种组合的两项研究一样(上表)。这些患者在巴塞罗那临床肝癌(BCLC)分期系统中被认为是晚期HCC,但我们知道这一人群的异质性【Hsu CY 2013】,这种状态可能与肿瘤负担无关。一些作者建议对这一人群进行重新分配【Giannini EG 2018】。鉴于以往研究的失败,TACTICS试验的结果并不令人惊讶。因此,由于在过去几年中缺乏共识和 2018 定义“不成功的TACE”的挑战,作者提出了另一种药物管理方法和对进展的新定义(图1)。 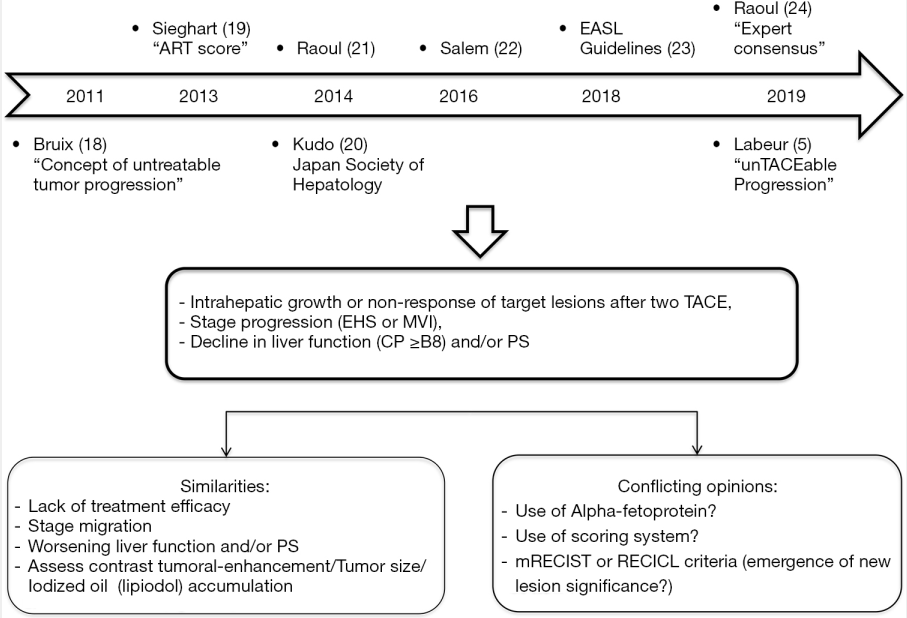
在药物管理方面,TACE抗血管生成治疗的时机是一个关键特征,可能是导致这一结果的原因之一。与其他研究相比,索拉非尼在第一次TACE前2至3周开始使用,试图降低VEGF上调。在第一个评估这种关联的对照试验中,在辅助环境中给予索拉非尼并没有显示出益处【Kudo M 2011】。索拉非尼的日剂量为400毫克/天(其他三项研究为800毫克/天),包括再次升级的可能性,并且在先前的临床研究【Nishikawa H 2014 Iavarone M 2011】和临床前研究【Chuang HY 2014】中建议使用较低的索拉非尼治疗剂量,特别是其免疫调节特性。因此,停药率下降,索拉非尼治疗的持续时间大大延长。这种趋势出现在晚期HCC III期试验【Kudo M 2018】和现实研究【Raoul J 2019 Tovoli F 2019】中。索拉非尼因药物相关不良事件而停药的比率随着时间的推移而下降(急剧下降:38%;反映:<10%),而接受索拉非尼的HCC患者的中位总生存期(OS)增加(急剧增加:10.7个月;反思:14.2个月)。同样,Raoul【Raoul J 2019】和Tovoli【Tovoli F 2019】发现索拉非尼和OS的治疗时间随着时间的推移而延长,剂量调整更频繁。换句话说,随着时间的推移,索拉非尼的管理得到了改善。
在TACTICs试验中,在证明肿瘤存活或适合cTACE的局部和/或远处肝内复发的患者中,重复的cTACE疗程可以进行,而这是疾病的自然过程。Kudo等人使用了不同的进展终点,满足肝癌反应评估标准(RECICL)和日本肝病学会(JSH) TACE失败/难治性标准(15)。这是对样本量研究的主要批评之一,但直到现在,进展的定义还不清楚。此外,这种再治疗政策与目前的做法是一致的。Bruix等人(18)首次引入了无法治疗的进展(肝功能和/或PS的主要进展或下降)的概念。几年后,TACE失败(缺乏治疗效果)/难治性(肿瘤恶化(增大/增大)或分期转移)的概念出现在亚洲和欧洲的指南中。此外,其他研究建议使用评分系统(19)来决定是否应该继续进行TACE,或者对“不可tacable进展”进行新的定义(图1)。
无进展生存期(PFS)作为中期HCC的主要终点得到了目前可用的后续治疗方案的支持,这使得仅基于OS评估TACE的益处变得更具挑战性。进展后生存期延长可能混淆OS估计。因此,本研究(15)和其他研究(5)都支持使用新的终点,如“不可治疗进展”的时间,作为治疗指导和未来的试验。
另一点值得一提的是,TACTICs试验的有效率和PFS都非常高,特别是单独cTACE组 。这再次提出了在这个异质性中间阶段谨慎选择患者的问题。换句话说,我们是否应该使用TACE和索拉非尼联合治疗整个患者群体?这项研究提出了新的见解。TACE后的完全缓解标准是已知的,而一些中期HCC患者显示出更高的复发风险,而其他患者可能无法从TACE中获益,因此可能需要更早开始全身治疗。Wang等人【Wang Q 2019】提出的“6 & 12”评分(肿瘤大小和数量的总和)可以将推荐的TACE候选人的生存进行分类,使用简单的风险分层分为三个亚组。此外,这种新模型具有明确的界限,不像根据7 - 7个标准(内/外)划分肿瘤负荷的中期亚分类,可能减少了可以从TACE获益的患者范围。
总之,这项研究提供了意想不到的结果。索拉非尼仍然可以作为主要的治疗选择,因为它具有vegfr抑制特性。它概述了一种有吸引力的联合治疗方法,这正在成为晚期HCC的新标准。其他重要的结果尚未公布,TACE影响免疫微环境,并可能增强免疫检查点抑制剂的作用。我们的实践将不断发展。如果这些发现得到支持,指南将必须更新,以整合这些结果,并指定可能从中受益的患者类别。
未读文献 Jingxin Yan # 1 2, Yonghao Wen # 1 3, Manjun Deng 1 2, Bin Ye 4, Xinlian Liu 5, Lushun Zhang 5 Transarterial Chemoembolization Plus Sorafenib versus Transarterial Chemoembolization Alone for Advanced Hepatocellular Carcinoma: An Umbrella Review of Meta-Analyses and Systematic Reviews J Hepatocell Carcinoma . 2023 Oct 5:10:1723-1733. doi: 10.2147/JHC.S429352.
Sorafenib plus transarterial chemoembolization vs sorafenib alone for patients with advanced hepatocellular carcinoma: A systematic review and meta-analysis. Yang HJ, Ye B, Liao JX, Lei L, Chen K.World J Hepatol. 2024 Jan 27;16(1):91-102. doi: 10.4254/wjh.v16.i1.91.
|