TACE是一种利用正常肝实质和肝细胞肿瘤之间解剖上的血供差异来治疗HCC的微创方法。与正常肝实质相比,这些肿瘤的代谢增加,因此必须促进血管生成以增加血流量,以满足增加的代谢需求。正常肝实质主要由门静脉系统供血,而肝细胞性肿瘤主要由肝动脉系统[24]供血。这一解剖差异使我们能够通过肝动脉供血通过TACE靶向递送治疗药物,同时保留健康肝组织【Roayaie, S. 2015】。
根据给药部位的不同,TACE治疗方法有肝叶、选择性和超选择性。在肝叶给药时,治疗药物被输送到肝动脉的肝叶分支,从而将药物输送到包含HCC的整个肝叶。相比之下,选择性和超选择性TACE技术通过直接将药物给予段动脉(选择性)或亚段肝动脉(超选择性)来提高化疗的精确性。与肝叶TACE相比,选择性/超选择性TACE显示出更高的肿瘤坏死水平(75.1%对52.8%,p = 0.002)。总体而言,选择性和超选择性TACE显示完全缓解率为40% ~ 50%【Albrecht, KC. 2021】,5年总生存率为20% ~ 30%【Malagari, K.2012】。
在TACE治疗中,除了解剖位置的变化外,还有两种主要的给药技术:传统TACE (c-TACE)和载药微球TACE (DEB-TACE)。在c-TACE中,碘化油化疗药物通过进入肝动脉的导管输送到肿瘤,然后是栓塞剂。这种方法增加了肿瘤内的化疗药物浓度,同时最大限度地减少了药物洗脱【Kis, B.2017】。此外,与c-TACE相比,DEB-TACE利用载药微球持续递送化疗药物,提高了标准化程度,并可能降低肝脏毒性【Melchiorre, F. 2018】。DEB-TACE和c-TACE均使用化疗药物栓塞肿瘤供血动脉,产生促进肿瘤坏死的缺血状态。c - TACE和DEB-TACE常用的化疗药物包括多柔比星、顺铂和丝裂霉素C【Makary, MS.2020】。传统上,这三种药物一起给药; 然而,最近的临床实践趋势越来越多地看到阿霉素作为单药治疗【Lu, J. 2021】。
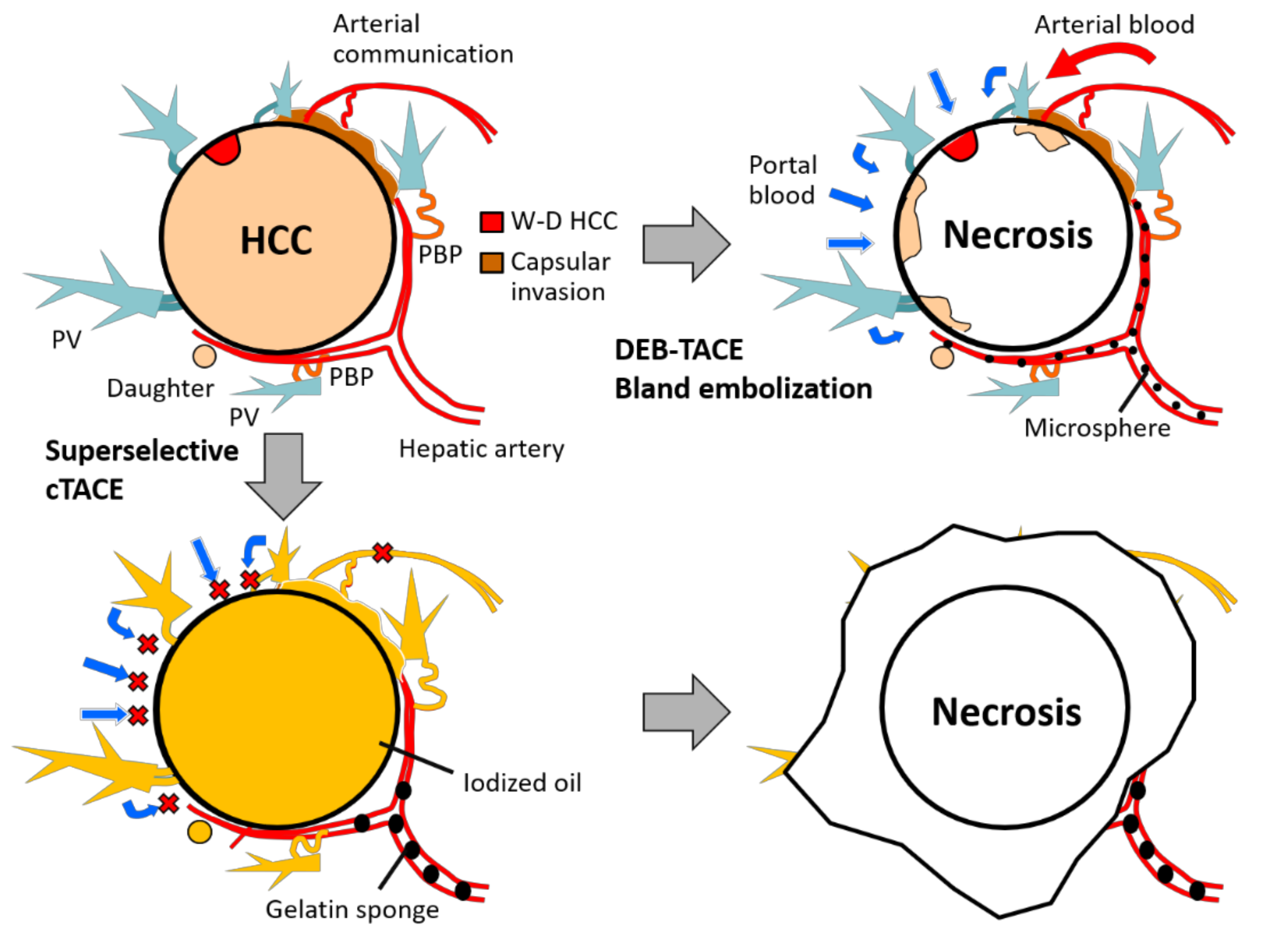 超选择性cTACE和DEBTACE/单纯栓塞(Bland embolization)的基本原理示意图 目前缺乏TACE治疗中化疗药物的选择和剂量的指南。目前使用的剂量范围多柔比星为10 ~ 100 mg,顺铂为10 ~ 100 mg,丝裂霉素C为2 ~ 30 mg【Lencioni, R. 2016】。TACE中使用的化疗药物的剂量可以根据体表面积、肝功能或体重确定,也可以根据经验确定。即使没有标准化的给药方案,DEB-TACE和c-TACE也显示出优于全身化疗的治疗靶向性【Boehm, L.M. 2015】。
TACE治疗中使用的所有方法(肝叶、选择性和超选择性)和技术(c-TACE vs. DEB-TACE)均已被证明是安全的,但存在若干已知风险。高达80%接受TACE治疗的患者会出现栓塞后综合征(PES)【Makary, M.S.2021】。PES包括无感染的栓塞后发热,以及腹痛、恶心或呕吐。虽然在TACE术后的患者中,PES很常见,但大多数PES病例在72小时内消退,极少数病例进展为严重的临床后果。大约5%的病例发生与TACE相关的罕见但严重的并发症,包括脓肿、急性胆囊炎、医源性夹层和急性肝衰竭【Blackburn, H. 2016】。
|

