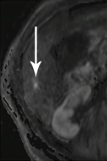
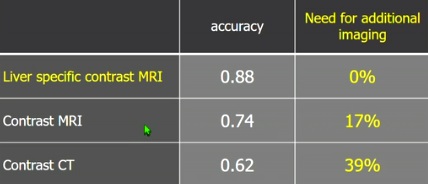
Ӱ��ҽ���Ĺ۵���֢Խ��ԽС cancer are getting smaller.....�ִ�Ӱ��ѧ���Է��ֺͼ���4mm��С�Ķ��Բ���
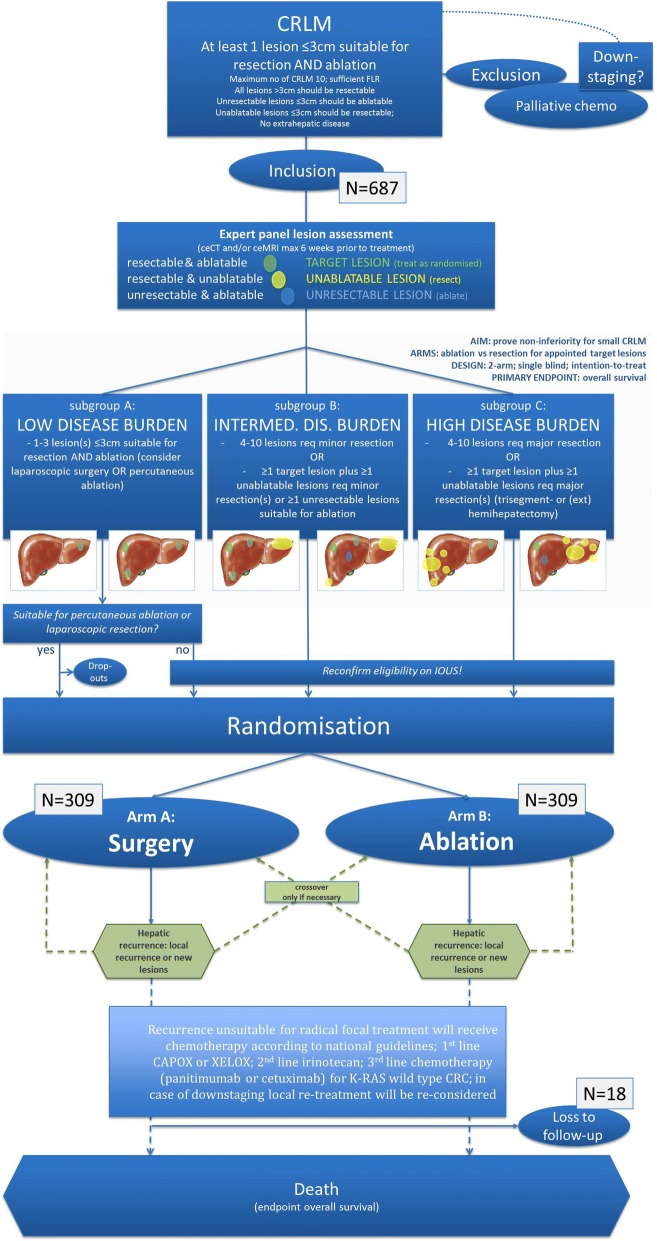
ʵ������С���䣨paucilesional��ҲԽ��Խ����Ӱ�����������Ƶ�ְȨ��Χ��  meta���� ���������Է���CT��MRI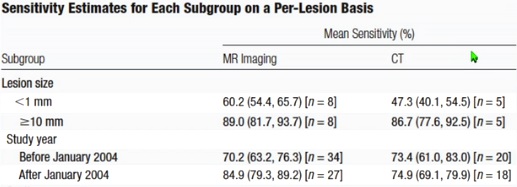 �������ԽǶȽ�MRI��CT ����������Ӱ����Primovist��
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
 |
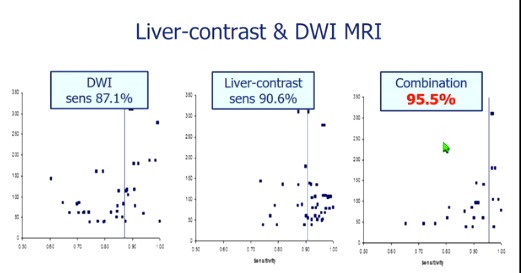
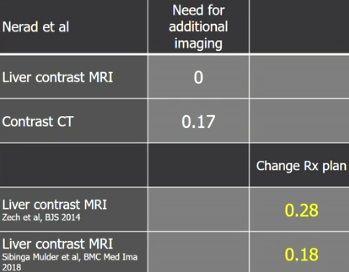
����������Ӱ�������²��䡣������complementary��
����������Ӱ��MRI��Ϊ��ʼ����ʽ�������������CE-CT��CM-MRI������������Ӱ����ǿMRI�鲻��Ҫ��һ����Ӱ��ѧ��飬�����Ч�����ıȽ���ʾ����������ǿMRI����������ơ�
FDG PET-CT
Meta������2010����ǰ��PET≈MRI ������Ϊ80%
ǰհ���о���2019�꣩ PET-CT������70% ����MRI 85%��������
��Լ20-30%PET-CT��ı������Ƽƻ���
���������� CT ������������ CT Texture
��������ָͨ��һ����ͼ����������ȡ�����������������Ӷ���������Ķ������������Ĵ������̡��������������������ʶ��ԣ��ɷ�Ϊ4���ࣺͳ�Ʒ����������ṹ�����������źŴ���������ģ�ͷ�����
������������Ԥ�����ڽ�ֱ����ת�Ʒ���≤6���£������Ƕ������ٴ�������һ�����õĸ����ֶΡ�
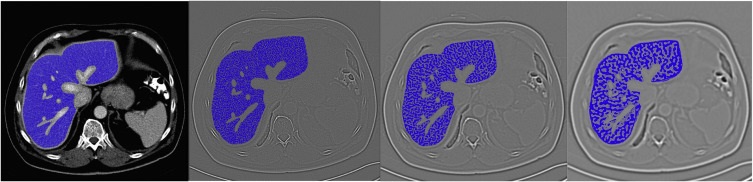 |
|||
| (a)û�й��� | (b)ϸ���ˣ�0.5�� | �еȹ��ˣ�1.5��(c) | �ֹ��ˣ�2.5��(d). |
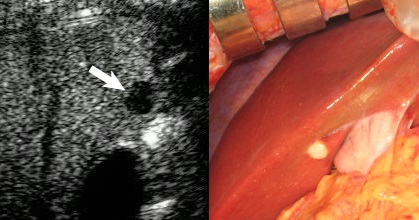
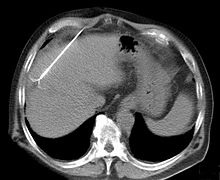
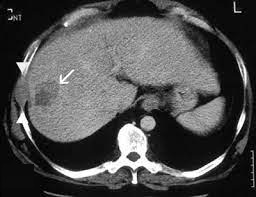
����������
���ڽ�ֱ����������Ҫ���ز�CT����CT
PET-CT���������ڵ�ɸ���ֶ�
��ȷ���ķν�ڲ��䣺ֻ�������CTʱ������������ſ�����Ϊת���Խ��
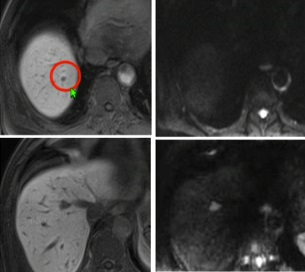
���ƻ���ֱ������ת�Ƶ�����ʱ������CT��ɸ��ֱ�ӷ��ָ���IJ��䣩����������Ӱ��MRI+DWI��������95%�����Գ���CT���ܷ��ֵĸ���IJ��䣬��PET-CT���Գ������ת�ơ�
���ڸ�������������϶�����Щ�仯��
�����ڿƣ�ʲôʱ��ֲ��������������������ٴ��Ϻ;�������Ч��
Ӱ��ѧ��������һ��С����ʱ��������������ԣ�
��ƣ���һ������Ļ��߷�����Ҷ���Ų�С����ʱ������ƣ�
�������룺�Ƿ��������������һ�����Կ�Ԥ���ԺͿɿ������ƻ��������ƣ�
������ΪĿ�ĵĽ�ֱ������ת�Ƹ����ٴ�רҵ�������Լ��Ĺ۵�
 |
|
 |
 |
 |
|
 |
 |
�����ڿ�ҽ���Ĺ۵� The oncologist's point of view
��ֱ�������г����ڹ�����ת���Բ��䣬Ŀǰ�����ֵ��͵�̬��
̬�� 1. Wait & Watch �ȴ��۲�
☺
֧�ֵ�һ����̬����Ϊ��
- ���������ƽ���������������Ч��
- ��ʹ�Dz���������even if not����ȫ�����ƿ�������ת�ư������ӻ��Ƶ�ʱ��Ҳ�Dz��ɱ���ģ�inevitable��
- �����Ҫȫ���¸���������Ͼֲ����ƣ�Ԥ��ͳ�ʼ�ֲ���Ԥ��һ����
֧�ֵڶ���̬����Ϊ
- ȫ�����ƿ��ṩ�г��ڿ���OMD
- ����������ƣ��ر��ǿ��ǵ��������2/3����OMD����ΪPMD��progress metasteses disease����
- ���湦�ܸ���֯
�����ڿ�ҽ����Ĺ�ʶ
- �ɽ���������ΪĿ�ĵľֲ���Ԥ����
- ���ǣ�Ԥ������������DFl��disease free interval������Ъ�ڣ���ͬ��ת�ƣ�����ת�ơ��ι��ܲ�����һ���������ϵ�ת��
- Ȼ���˾�����ʼȫ�����Ƽ�/���ֲ���Ԥ
�������ϣ�����Ҫ�ģ�above all��
- ��Զ��Ҫ����������
- ��ϵģ�upfront����ѧ�����ƻ�������ѧ������
 |
 |
��Ȼ����δ�����������Unmeet needs��
ȱ��ʵ֤�Ƚ����ݣ�����ȱ���ɿ��ıȽ�����
- ��OMD��������ת���Բ��䣩�н��в�ͬ���͵ľֲ����ƱȽ�����
- ���Ͼֲ��������������ȫ�����ƵıȽ�����
���ҽ���Ĺ۵�
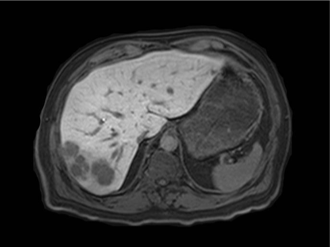 |
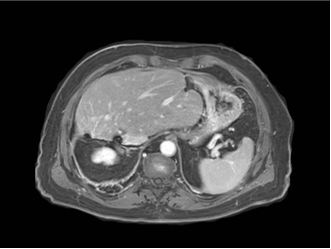 |
| �ž���˨�� | �Ҹβ����г���2.5�����Ժ� |
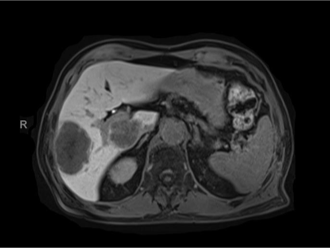 |
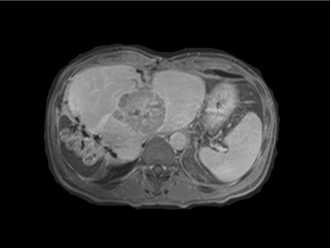 |
| �ž���˨�� | �Ҹ��г�19�����Ժ� |
 |
| �����г��ĸΰ� |
 |
 |
|
Right lobe dominant ��ҶΪ��
|
Left Lobe ��ҶΪ��
|
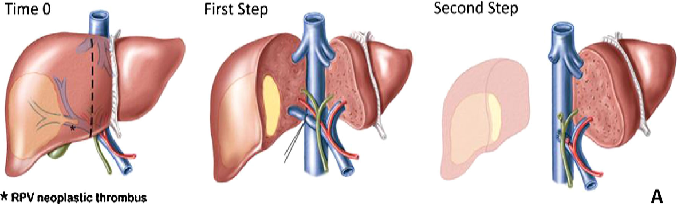 |
�����г�
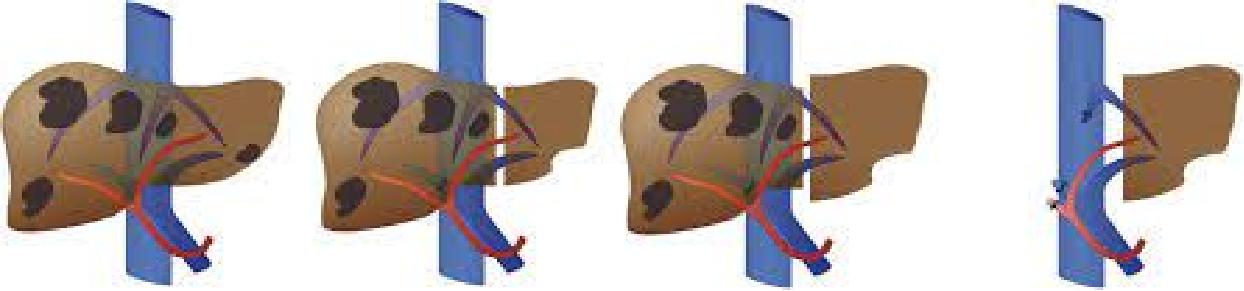 |
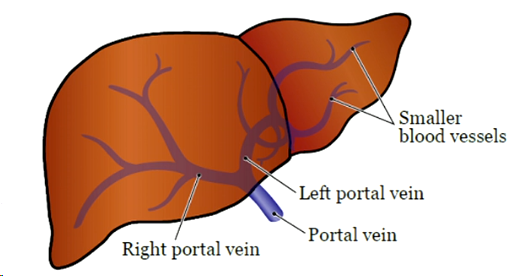 |
| �ž������� |
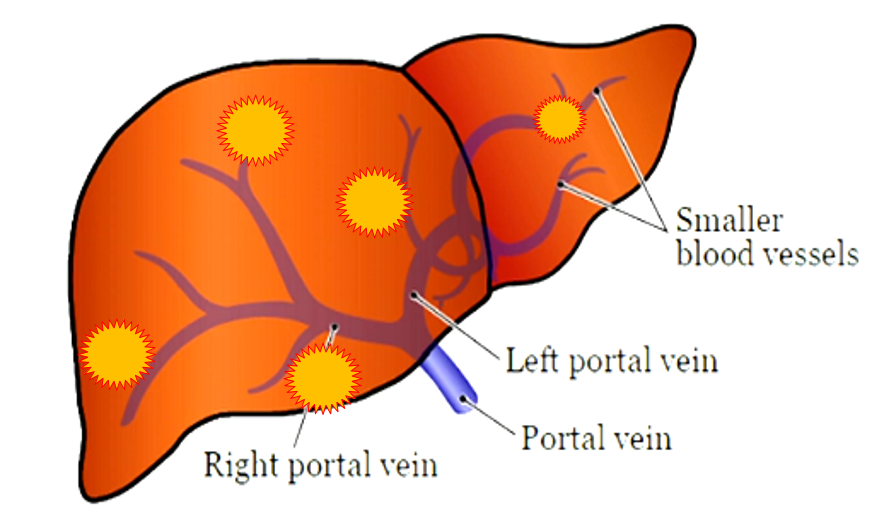 |
|
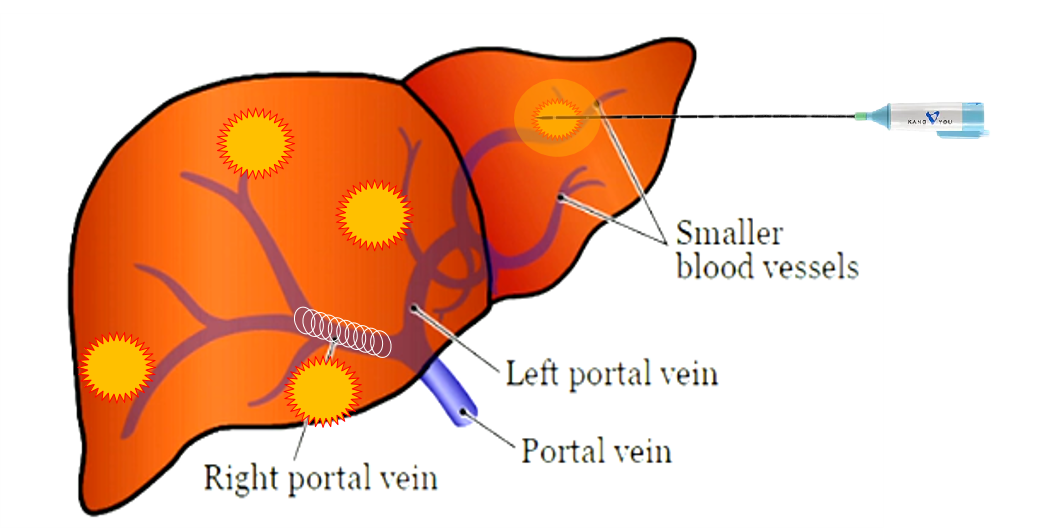
�Ҳಡ��Ϊ�����������������ƣ��Ҳ��ž���˨��ͬʱ��ಡ����������
|
 |
|
�Ҳ��ž���˨����ͬʱ��������ಡ�����������
|
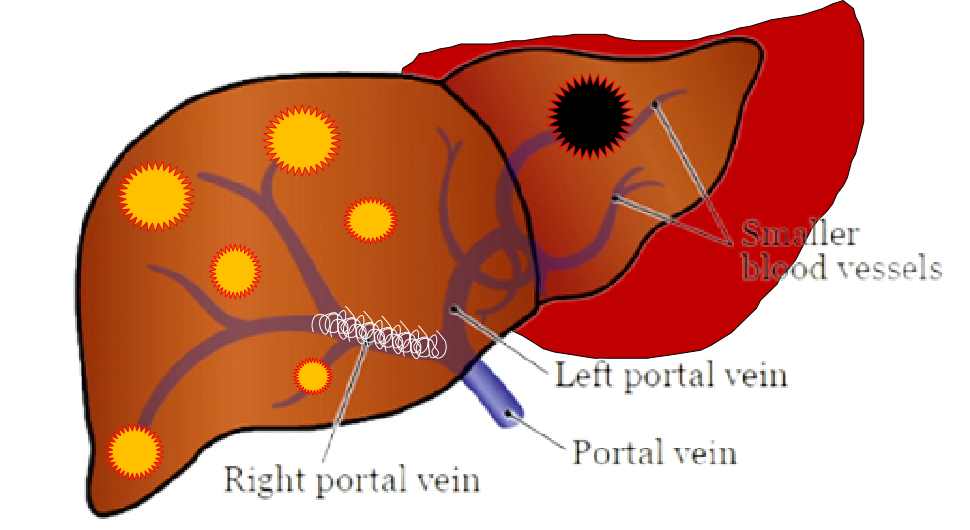 |
| �Ҳ��ž���˨�����Ե���δ��������ݻ����� |
 |
|
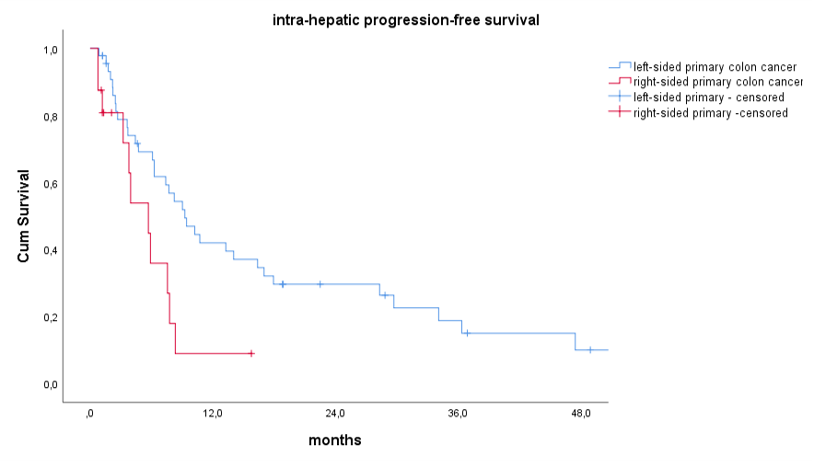
Median ihPFS for patients with a left-sided primary tumor was 9.3 ±1.6 months vs. 5.7 ± 1.5 months patients with a right-sided primary tumor (p=.013)
|
 |
|
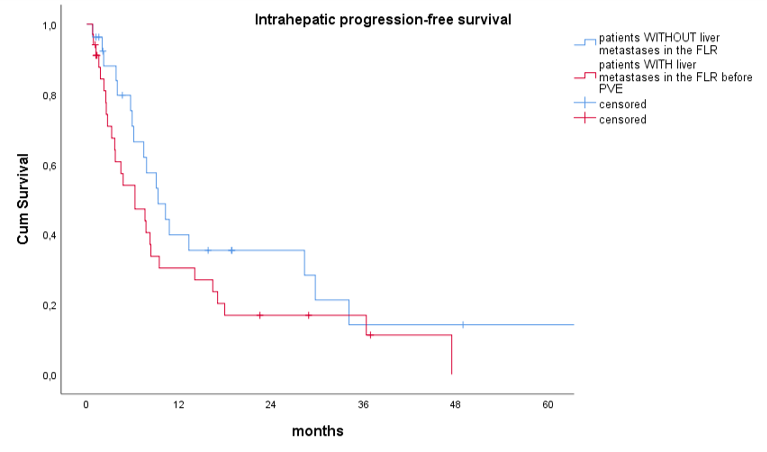
Median ihPFS in patients without metastases in FLR: 9.3 ±2.1 months vs. Patients with metastases in FLR 6.2 ±1.9 (p=.115)
|
- CRLM���ߵ�ihPFS������ԭ������λ�õ�Ӱ�� �����᳦Ч�������Ұ�᳦��
- ����ֱ�������ߵ���λihPFS���Ҳ�ԭ���������߳�3.6����
- ��PVE���г�ǰ��FLR�д��ڸ�ת�Ʋ���Ӱ�������չ������
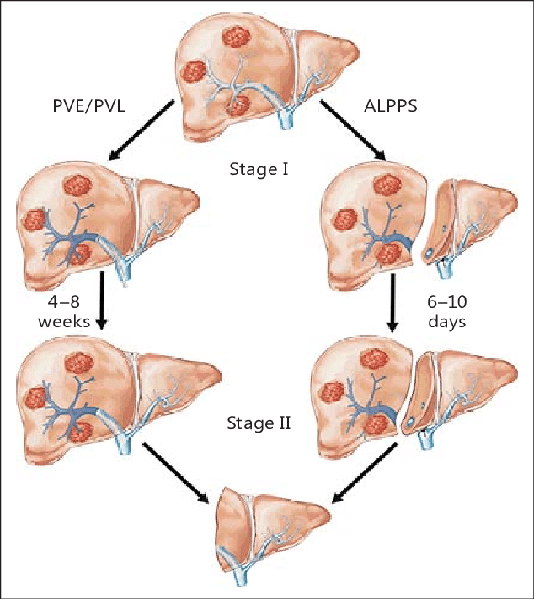
2. ALPPS
���ڸ��г����иηַָ�ָ������룩���ž�������������Ӧ��
·���ߵ�������
·���óɱ�
 |
|
��һ���������ž������� ��ʵ���г�
�ڶ�����������ȫ���г�
High morbidity/mortality |
������ALPPS �ž����������ž���˨������������г����������������̽����һ��̽�������
����ҽ���Ĺ۵�
�������ѧ�ڽ�ֱ������ת�ƾֲ����ƵĽ�ɫ����
1. ���� Cure
����
 |
 |
 European Organisation for Research and Treatment of Cancer
European Organisation for Research and Treatment of CancerCLOCC�о�
��Local Treatment of Unresectable Colorectal Liver Metastases: Results of a Randomized Phase II Trial��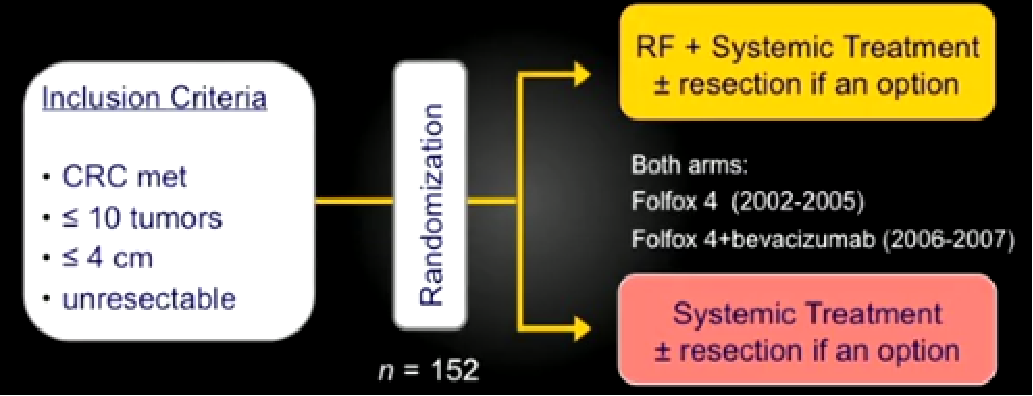
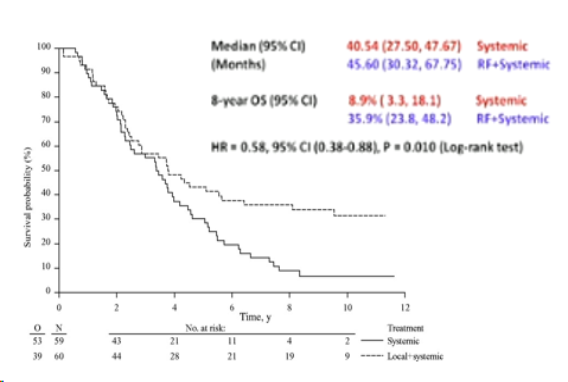 |
| �����г��Ľ�ֱ����ת�ƻ��߽���ȫ�����ƻ�������Ƶ����±�г�����������Kaplan-Meier����(P=.01)��Pֵ����˫������ȼ�����м��㣨�����ͼ��ȫ���� |
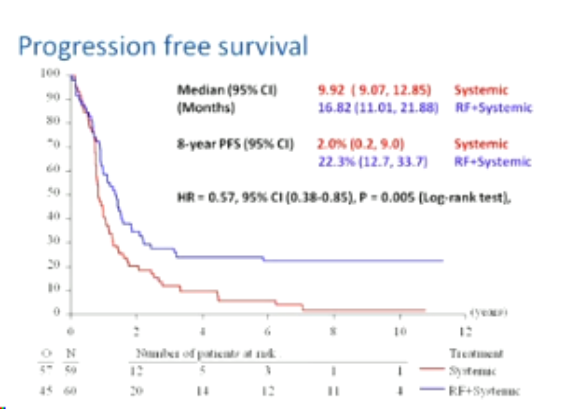 |
| �����г��Ľ�ֱ����ת�ƻ��߽���ȫ�����ƻ�������Ƶ����±�г�����չ�����Kaplan-Meier����(P=.005)��Pֵ����˫������ȼ�����м��㡣 |
��һģʽ���磺�������ѧ�ֲ�����+���

ESMO consensus guidelines;Ann Oncol 2016

 |
 |
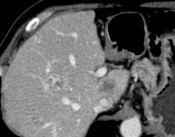 |
| left lateral sectiorectomy |
segmentectomy
|
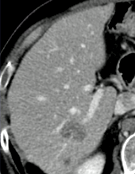 |
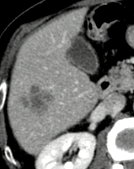 |
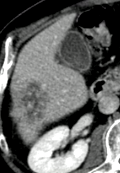 |
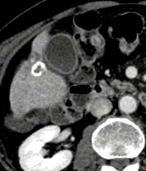 |
|
segmentectomy
|
segmentectomy
|
segmentectomy
|
segmentectomy
|
һ������
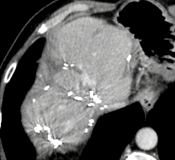 |
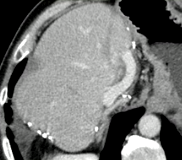 |
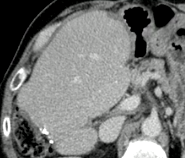 |
 |
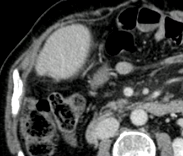 |
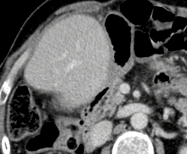
����������ڱȽϵ�ϵͳ�ع˺����ͷ���
SURGERY VERSUS THERMAL ABLATION SYSTEMATIC REVIEW AND META-ANNALYSIS
- Surgery is superior to RFA alone ����������ڵ����� RFA
- Ablation was only employed for unresectable disease! ���ڽ��ܹ����ڲ����г��Բ���
- Conclusions: ���ۣ�"The apparent selection bias from previous studies and the superior safety profile mandate the setup of RCTs comparing ablation to surgery." ������ǰ�о�������ѡ��ƫ�к���Խ�İ�ȫ�ԣ�Ҫ������������о��Ƚ����ں��������
��� vs �����ڣ�Collision ����
SURGERY VERSUS THERMALABLATION�� COLLISION TRIAL
PERCUTANEOUS RFA IN MCRC FACTORS AFFECTING OUTCOMES
- Tumor number √
- Tumor size> 3cm √
- Presence and number of nodal mts √
- Extent of EHD √
- Disease-free interval from primary resection ×
- CEA levels ≥ 30ng/mL ×
- KRAS mut ×


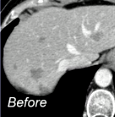
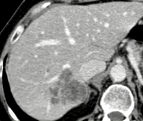
����ֱ�������ڣ��¸�����Downsize
 |
 |
 |
 |
Test Biology
 |
 |