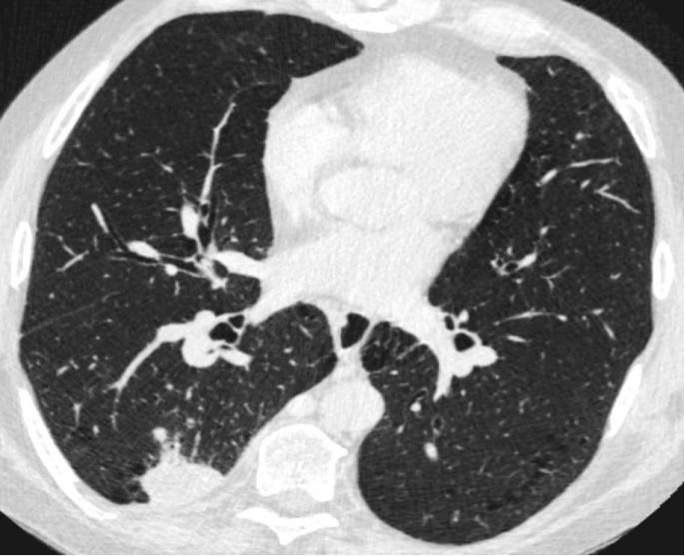
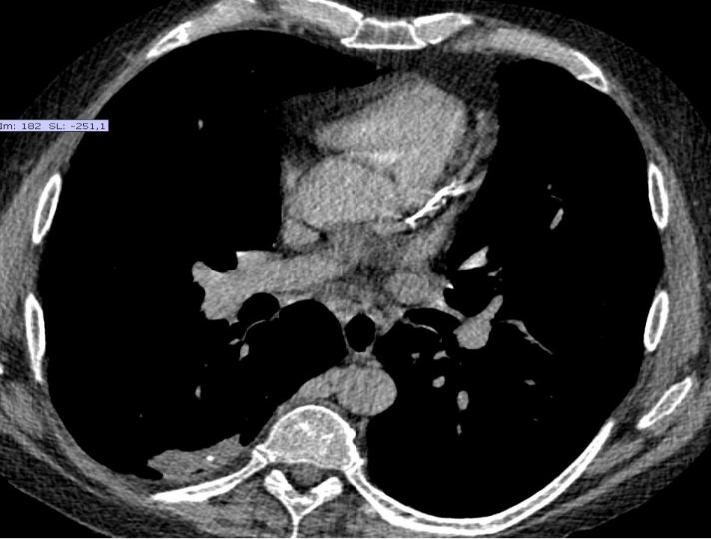
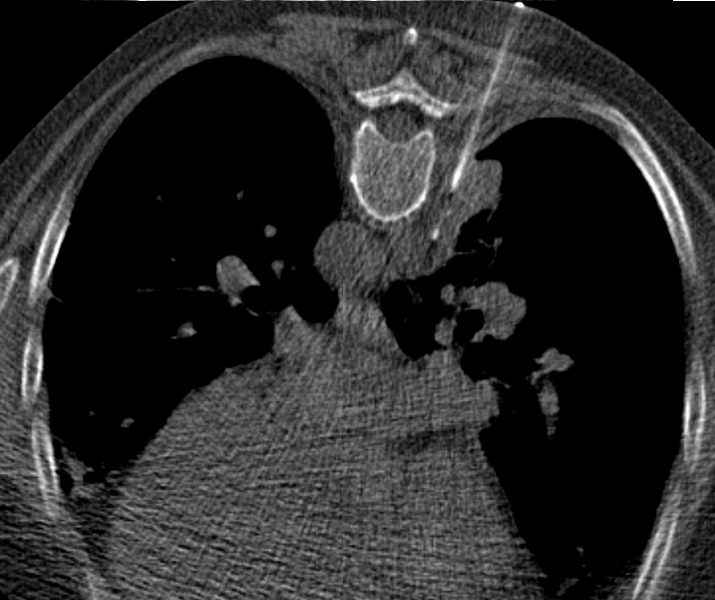
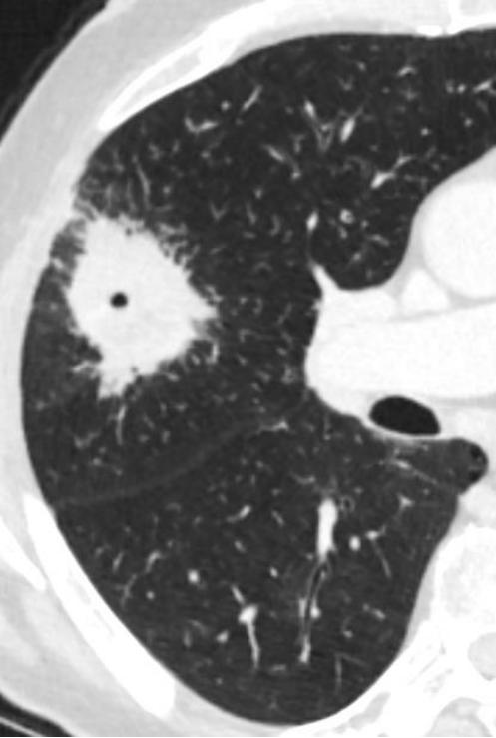
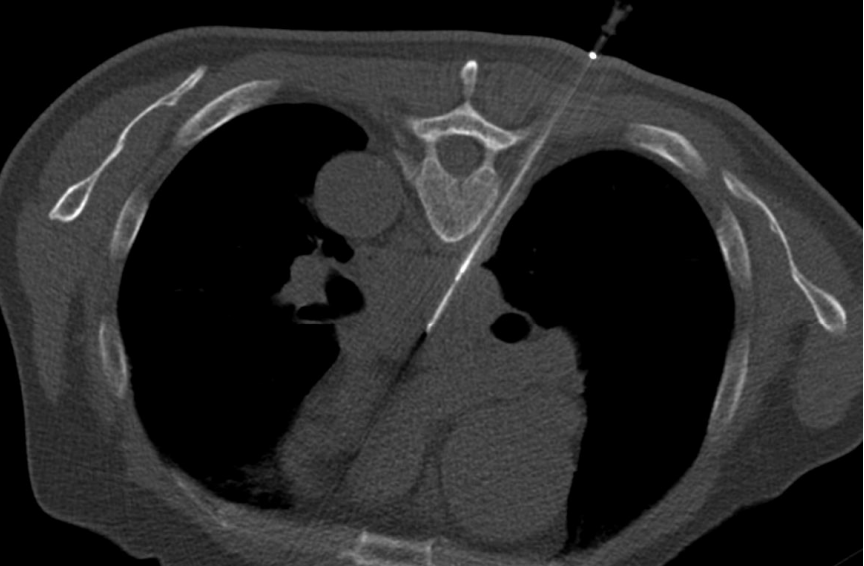
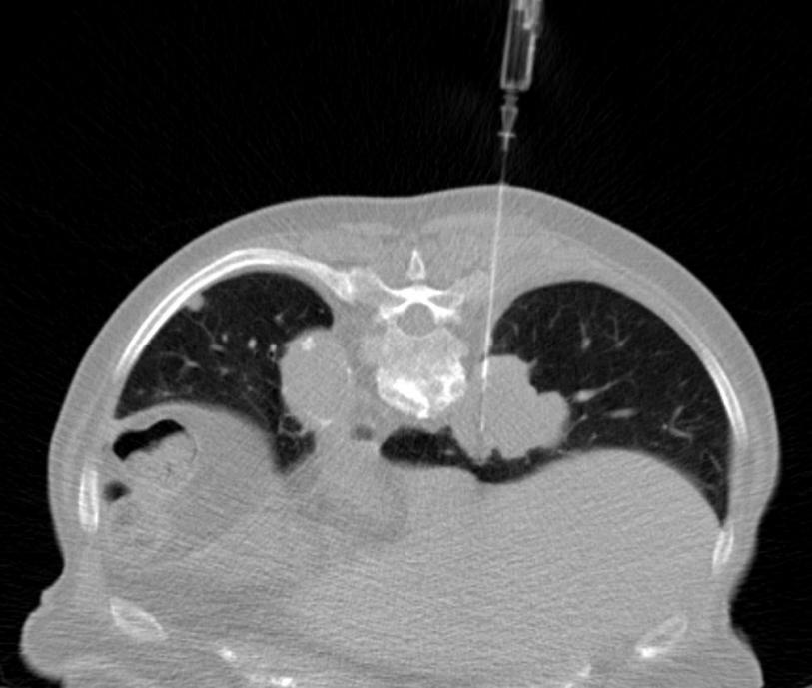
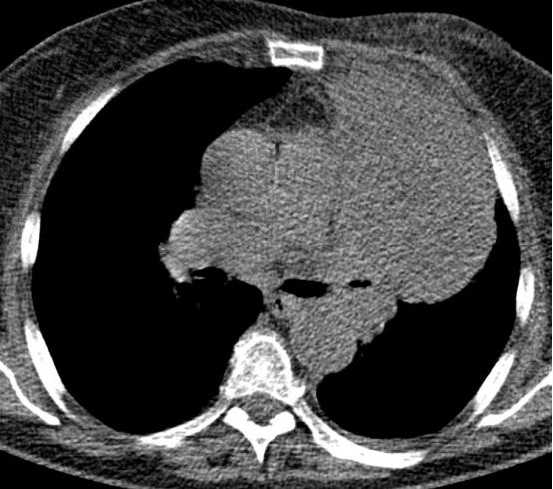
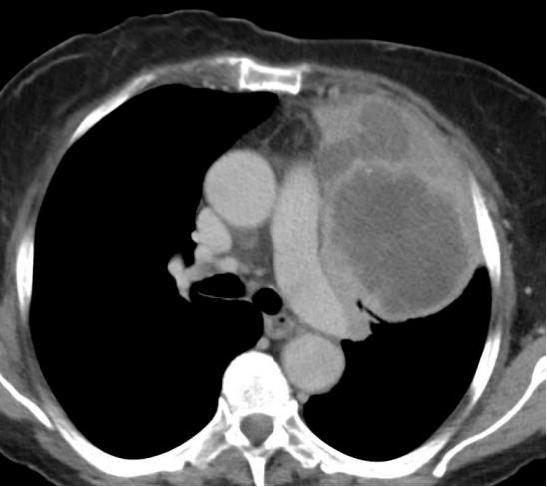
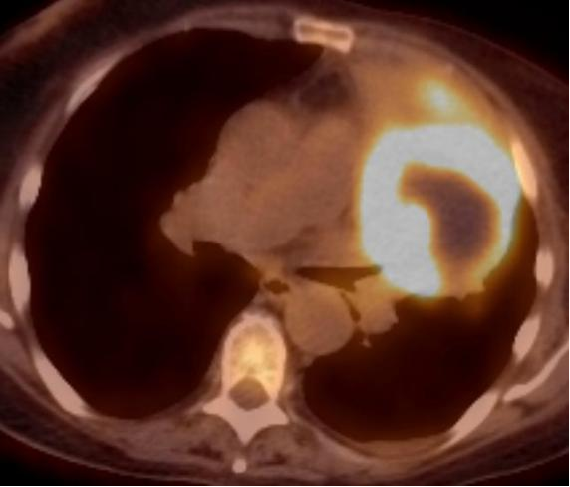
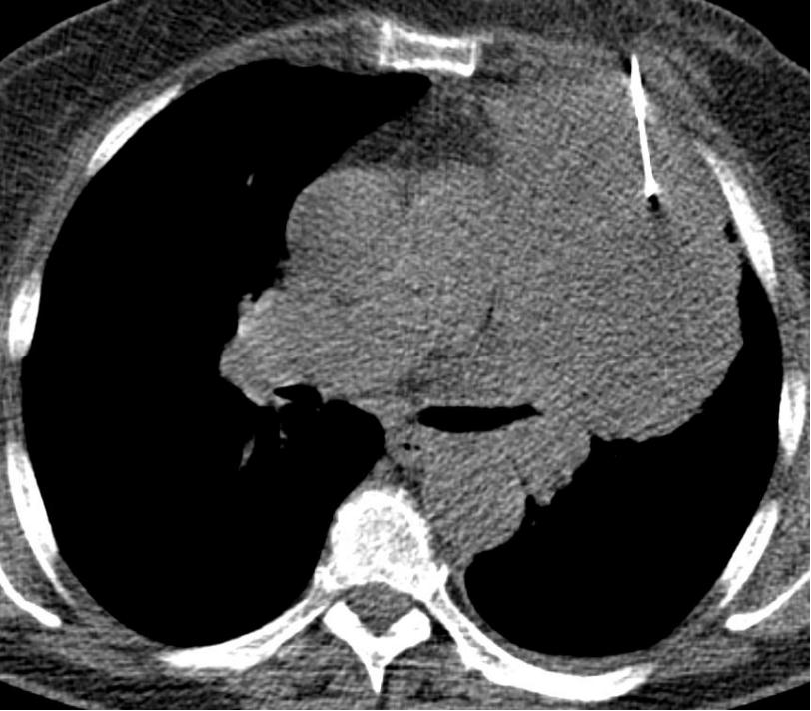
经皮肺活检的适应症经皮肺活检的主要目的是完成可疑肺部病变的最后诊断包括 To establish a final diagnosis of a suspicious lung lesion
为了最大限度地降低患者的风险,同时使他们的利益最大化,活检必须
(1)是活检适应症 (2)对患者安全 (3)技术上可行 (4)最可能产生诊断结果 (5)活检的风险和好处必须与其他侵入性和非侵入性管理方案进行权衡。、 经皮肺活检的主要适应症包括下列
肺穿刺活检最常见的指征是评估扩大或持续的肺结节是否为原发性或转移性恶性肿瘤。在这种情况下,针活检可以确认诊断,并为靶向治疗所需的分子分析提供组织【Jamshidi 2017;Kim ES 2011】,活检可在整个治疗过程中重复多次,不会增加并发症【Fintelmann 2019】。对治疗无反应的疑似感染患者也可能受益【Kiranantawat 2019】。细针抽吸活检可以识别特定的微生物,排除恶性肿瘤和非感染性炎症过程等。其他诊断虽然通过针活组织检查可以确认错构瘤等良性病变,但这一任务不可避免地需要更多的组织。
由于纵隔内非癌肿块占相对优势,当切割针同时获取常规细胞学标本以及组织学标本时,针吸活检的精确性显著提高。最好的例子是对淋巴瘤的诊断。据报道,仅用细胞学对非何杰金淋巴瘤诊断,其敏感性范围为54-83%。加用组织学之后,超过90%的病例可获得诊断和分型。细胞学和组织活检都不能可靠的鉴别非何杰金淋巴瘤中的滤泡型和弥漫型,但这并无太大的临床意义。对非何杰金淋巴瘤诊断的总体结果较何杰金氏病更优,由于后者的诊断试验是相对较少的Reed-Sternberg细胞的形态。组织学标本对胸腺瘤的诊断也具有优越性,虽然鉴别良性和恶性可能比较困难。对于纵隔癌性肿块的诊断,细胞学检查较为成功,但加用组织学检查有益于精确的分型,尤其在之前的组织标本不能用于比较时。
对于肺部恶性肿瘤,仅用细胞学检查就可能成功,据报道其恶性敏感性为80-93%。当获得适当的组织学标本,联合检查的恶性敏感性增加至85-97%。虽然细胞学足以鉴别小细胞肺癌和非小细胞肺癌,但加用组织学有利于精确的亚型确定。特别是当今精准医学分子靶向药物治疗需要组织学标本进行基因检测。组织学检查最为显著的优点在于,对于良性结节能够获得特异性的诊断。如果获得特异性的良性诊断,则阴性预测值可达到100%。对于良性疾病,仅用细胞学检查只能提供非特异性的非癌的结果,在这种情况下,阴性预测值会低很多。因此,通过重复活检或者手术进一步诊断往往是必需的。
针吸活检也可用于对弥漫性肺间质病变的诊断。在大约75%的弥漫性感染中,仅用细针穿刺细胞学检查能够提示病因学因素,但在非感染性间质疾病中则不理想。对于非感染性疾病,使用大切割针能够提高精确性,但同时可出现较高的并发症发生率。不仅气胸更加多见,而且在高达21%的病例中可出现明显的咯血,据报道死亡率可达1%。在某些病例中,对于感染性疾病的诊断,同时患者并没有机械正压通气的情况下,细针穿刺活检似乎是一种可接受的选择。在大部分病例中,支气管镜和胸腔镜都更为精确和安全,应作为诊断手段的首选。
胸腔穿刺的并发症,除气胸外,还包括咯血和空气栓塞。据报道, 2-12%的病例可发生咯血。虽然通常是轻微和自限性的,但在极少数病例中,咯血也可以极为严重甚至致死。当横贯大气道或血管时,咯血则更为常见和严重,因此在肺门活检时其发生率大为提高。出血性疾病和肺动脉高压被认为是活检的相对禁忌症,由于其存在更严重出血的潜在危险。
可能发生空气栓塞的情况包括:在支气管与血管交通,同时胸内压力增高,包括咳嗽或正压通气时,或者在针与空气相通,而针尖在肺静脉中,同时胸内压力降低,如吸气时。这是一种极为少见的并发症,但却是致死性的。为了减少发生空气栓塞的危险,保证针头在病灶中是极为重要的,尤其在使用同轴引导针时。针进入胸腔的时间应尽可能缩短,并且不可与空气相通。对于活检过程中不能暂停呼吸的患者,这些预防措施更为重要。进行正压机械通气的患者不应进行经皮胸腔活检,除非在极为需要的情况下。
虽然透视可以在大部分早期胸腔活检研究中用于引导,但CT仍是目前最常用的手段。透视相对快速和简单,但仅限于可在二维平面中清晰观察的病灶,因此在显示纵隔内或接近纵隔的小结节或病变时较不满意。在透视引导下对胸膜基底的肺病变活检,当胸膜接触部位很小时,避免穿过正常通气肺则较为困难。阻塞后小叶塌陷可能会使中央型病变不明显,引起取样误差。 CT在确定最佳针刺路径方面更加精确,可以避免横穿通气肺和支气管血管结构。在纵隔内,往往可以通过横穿胸膜外路径到达病变。甚至当胸膜外的进入路径并不明显时,人工胸膜外开窗可以通过向壁层胸膜外注射生理盐水,来使相邻的通气肺从预期的针刺路径移位。对于胸膜肿物和周围型胸膜基底的肺部肿块,往往可以横穿胸膜接触部位,虽然偶尔需要通过复杂的方法。阻塞后塌陷也可用作为非通气途径进入中心型肿物。在CT引导下针尖可以更加准确放置在大小肿物中,因此能够避开肿瘤的坏死部分。手术者经验和高速CT扫描速度的提高,可以使CT引导胸腔活检的进行与荧光镜引导同样快速,而具有更高的精确性和安全性。
1. 除外恶性病变 excluding malignant disease
The National Comprehensive Cancer Network (NCCN), the American College of Chest Physicians (ACCP), and the American Society of Clinical Oncology (ASCO) have created guidelines for the diagnosis and treatment of lung cancer.
美国国家综合癌症网络(NCCN)、美国胸科医师学会(ACCP)和美国临床肿瘤学会(ASCO)已经为肺癌的诊断和治疗制定了相关指南。 The 2018 NCCN Guidelines for nonsmall cell lung cancer related to indications for percutaneous lung lesion biopsy advise the following category 2A recommendations:Patients with a strong clinical suspicion of stage 1 or 2 lung cancer (based on risk factors and radiologic appearance) do not require a biopsy before surgery.
2018年NCCN指南:非小细胞肺癌经皮肺病变活检相关适应症的建议 2A类推荐:患者有强烈的临床怀疑1或2期肺癌(基于危险因素和影像学)不需要术前活检。(可识别的早期肺癌不活检) A biopsy adds time, costs, and procedural risk and may not be needed for treatment decisions.
活检增加了时间、成本和程序风险,可能不需要活检就可以进行治疗决定。 A preoperative biopsy may be appropriate if a non-lung cancer diagnosis is strongly suspected that can be diagnosed by core biopsy or fine needle aspiration.
如果强烈怀疑良性病变或非肺癌的诊断可以通过活检或细针穿刺进行诊断,术前活检才可能是合适的。 A preoperative biopsy may be appropriate if an intraoperative diagnosis appears difficult or very risky.
如果术前诊断显得困难或非常危险,术前活检可能是合适的。 If a preoperative tissue diagnosis has not been obtained, then an intraoperative diagnosis (i.ewedge resection, needle biopsy) is necessary before lobectomy, bilobectomy, or pneumonectomy. 如果术前未获得组织诊断,则在肺叶切除术、双叶切除术或全肺切除术前,进行术中诊断(例如楔形切除和针吸活检)是必要的
The preferred diagnostic strategy for an individual patient depends on the size and location of the tumor, the presence of mediastinal or distant disease, patient characteristics (such as pulmonary pathology and/or other significant comorbidities), and local experience and expertise. 个别患者的首选诊断策略取决于肿瘤的大小和位置、纵隔或远处疾病、患者特征(如肺部病理和/或其他重大共病)以及当地的经验和专业知识。
侵入性最小的活检作为第一个诊断研究。 Anatomic pulmonary resection is preferred for the majority of patients with NSCLC.
大多数NSCLC患者首选解剖性肺切除术。 Patients suspected of having the metastatic disease should have confirmation from one of the metastatic sites if feasible but should have a biopsy of the primary lung lesion or mediastinal lymph nodes if it is technically difficult or very risky to biopsy a metastatic site.
如果可行,怀疑肺癌有转移性疾病的患者应从其中一个转移的部位得到确认,即如果怀疑肺内多发病变可能是转移过来的,应该考虑对其中的一个病变进行活检。但如果转移部位活检面临技术困难或非常危险,应对原发肺病变或纵隔淋巴结进行活检。 Patients with metastatic disease should have the histologic subtype established with adequate tissue for molecular testing (including consideration for re-biopsy or plasma biopsy) to enable the best guidance for chemotherapy options.
转移性疾病患者应建立组织学亚型的分析,并有足够的组织进行分子检测(包括考虑重新活检或血浆活检-plasma biopsy),以便为化疗方案提供最佳指导。 Decisions about the optimal diagnostic steps for suspected stage 1 to 3 lung cancer should be made by thoracic radiologists, interventional radiologists, interventional pulmonologists, and thoracic surgeons who devote a significant portion of their practice to thoracic oncology.
对于疑似1-3期肺癌的最佳诊断步骤应由肿瘤内科医生、介入放射科医师、放疗科医生和胸外科医生做出,这些医生其日常诊疗活动中应有很大一部分和胸部学相关。 Although they do not explicitly state it, the most recent ACCP guidelines carry the same general message as the NCCN guidelines that tissue diagnosis by the safest, least invasive means possible is the preferred route of proceeding in all patients with lung lesions.
尽管他们没有明确说明,但最新的ACCP指南与NCCN指南具有相同的信息,即通过最安全、最小侵入性的方法进行组织诊断是所有肺病变患者的首选途径。 The ACCP guidelines suggest that tissue diagnosis is required for chemotherapy/radiation decisions whether the lesions are "obvious" cancers or not.
ACCP指南建议,对于决定病变是否为明显的癌症,化疗/放疗都需要进行组织诊断。 However, the ACCP guidelines leave open the possibility that treatment can proceed without tissue diagnosis and favor endoscopic biopsy over percutaneous lung lesion biopsy when possible. 然而,ACCP指南保留了在没有组织诊断的情况下进行治疗的可能性,并在可能的情况下支持内镜活检,而不是经皮肺病变活检【Rivera 2013】。
The following ACCP guidelines related to indications for percutaneous lung lesion biopsy are listed below in nearly verbatim language.
作者强调,介入医生、胸外科医生、肿瘤内科医生或放疗科医生之间的共同决定是理想的方法。
对于基于影像学和临床表现的疑似小细胞肺癌(SCLC)的患者,建议病理诊断采用侵入性最低的方法 ( 痰细胞学、胸腔穿刺、细针穿刺(FNA)或经支气管镜穿刺,根据患者的表现(1C级)。
对于怀疑患有肺癌的患者胸外部位怀疑有转移,如果FNA或活检可行,建议获得转移部位的组织确认(1C级)。
对于怀疑有肺癌的患者,在多个远处病变怀疑转移,但转移部位的活检技术困难,建议采用微创方法对原发灶进行活检(1C级)。
对于怀疑有周围肺结节的肺癌患者,当由于诊断不确定或手术候选资格差而需要组织诊断时,推荐径向超声支气管镜(Radial Endobronchial Ultrasound )EBUS作为辅助成像方式(1C级)。
如果径向EBUS被认为不太可能实现诊断,那么如果设备和专业知识可用,则推荐电磁导航引导(1C级)。
备注:如果没有电磁导航,则建议进行经皮肺病变活检。
如果最初获得的标本不足以进行组织学和分子特征分析,那么考虑到准确的肿瘤特征分析的重要性,继续进行第二次活检是可以接受的。
在一个小(小于3厘米),孤立的,周围肺病变怀疑肺癌患者似乎早期疾病,是一个手术候选人,诊断困境通常围绕是否需要获得活检标本来确认癌症的诊断之前进行手术切除。
当病变是中度到高度可疑的肺癌时,通过胸腔镜进行的手术切除是确定诊断和确定治疗的最明确的方法。
对于恶性肿瘤可能性不确定的结节,可以考虑通过经皮肺病变活检或支气管镜检查取样,使用或不使用引导技术(桡动脉EBUS或电磁导航)。
ASCO指南对肺癌的管理影响,包括关于何时进行分子检测和哪些分子检测是可取的议题 【Kalemkerian 2018】。
然而,ASCO指南假设已经进行了组织取样,并且已经实现了癌症的组织诊断。(并无谈到活检的适应症问题)
介入放射学学会(SIR)指南(另一个栏目讨论)强调经皮肺病变活检的准备【Patel 2013】和其他方面的病人护理【Gupta 2010】PLLB,但不提供经皮肺活检的具体关于病人选择、基于病变特征的细节或决定和其他活检方法。
肺活检适应症 indication【Anzidel 2017】另外一个作者对肺活检适应症的表述
1. 新的活逐渐增大的实性孤立性结节或肿块 A new or enlarging solitary nodule or mass
这是影像引导肺活检最常见的适应证,一般人群中约8.5%的人偶然发现肺结节,有危险因素的受试者中高达50%的人偶然发现肺结节
如果结节最初在CR发现,既往CT诊断必须要看的,确定释放时新增结节
1. 病变特征
2. 估计恶性肿瘤的可能性
3. 确定活检的其他可及部位(胸外转移)
4. 决定是否进行肺活检
有其它类似肿瘤的良性病变,包括类风湿关节炎,结节病,结核和霉菌病等,需要活检以除外恶性病变。
3. 局灶性肺实质侵润性病变不能除外感染 Focal parenchymal infiltrates in which an infectious organism cannot be isolated
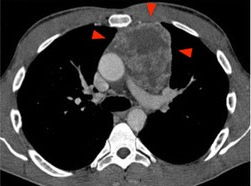
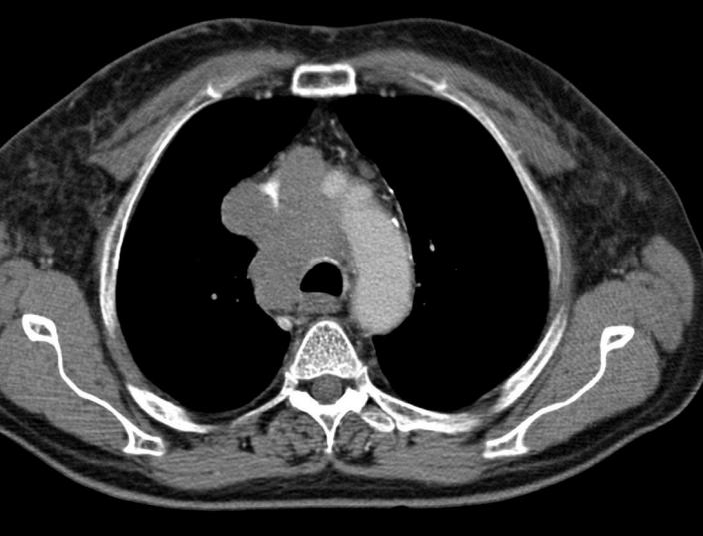
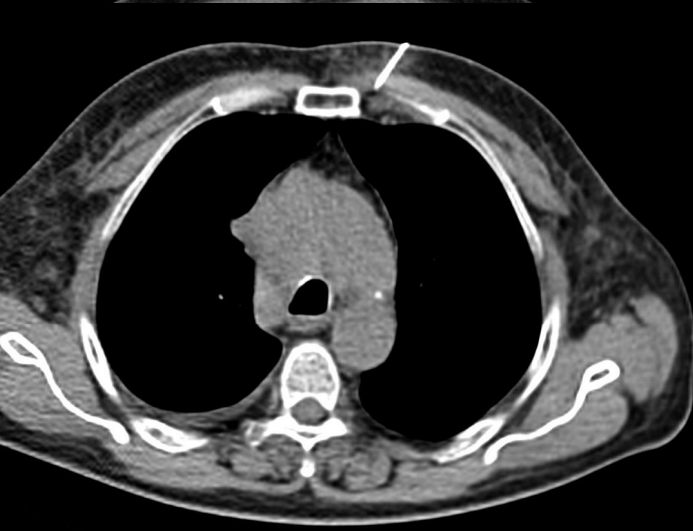
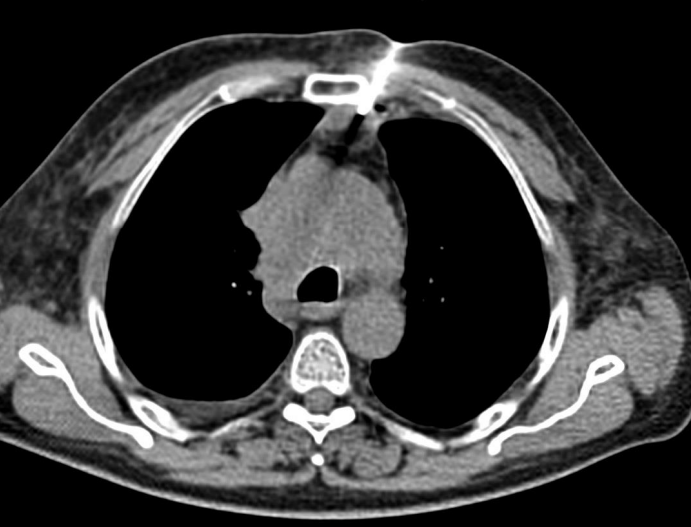
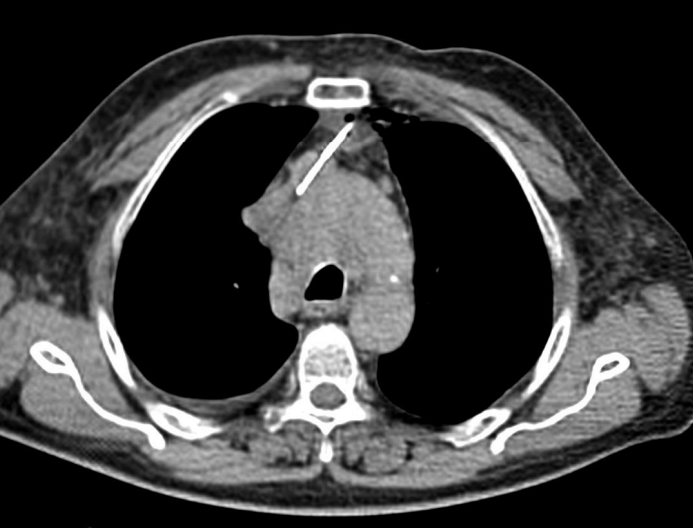
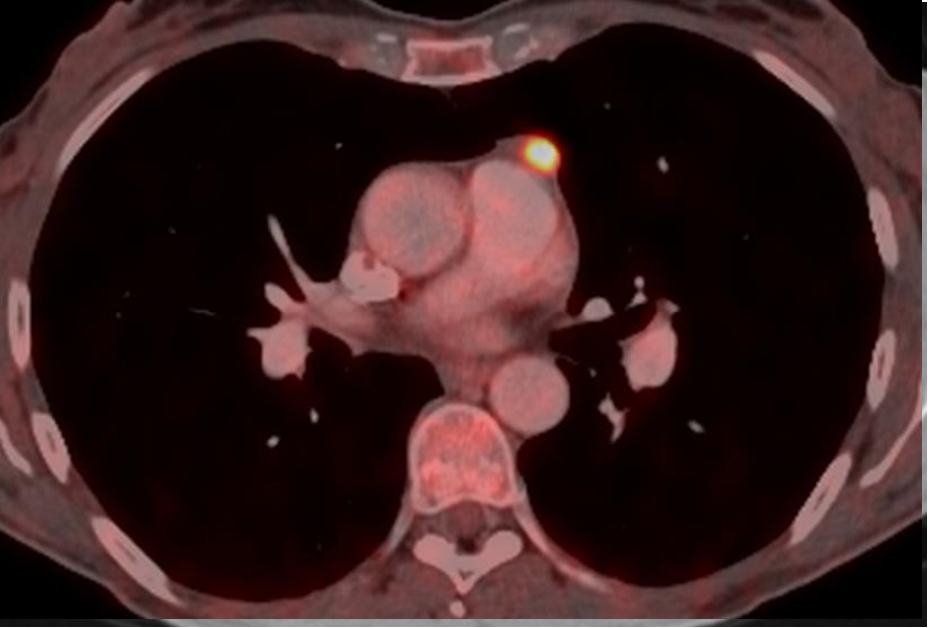
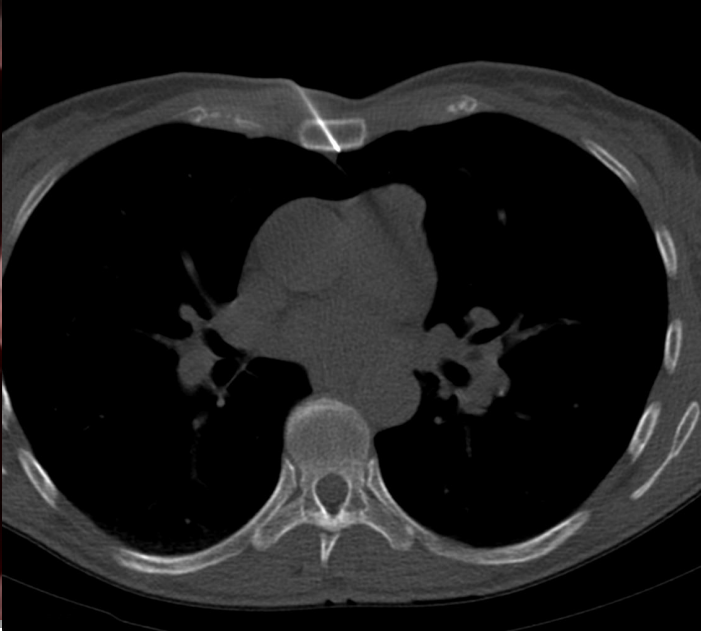
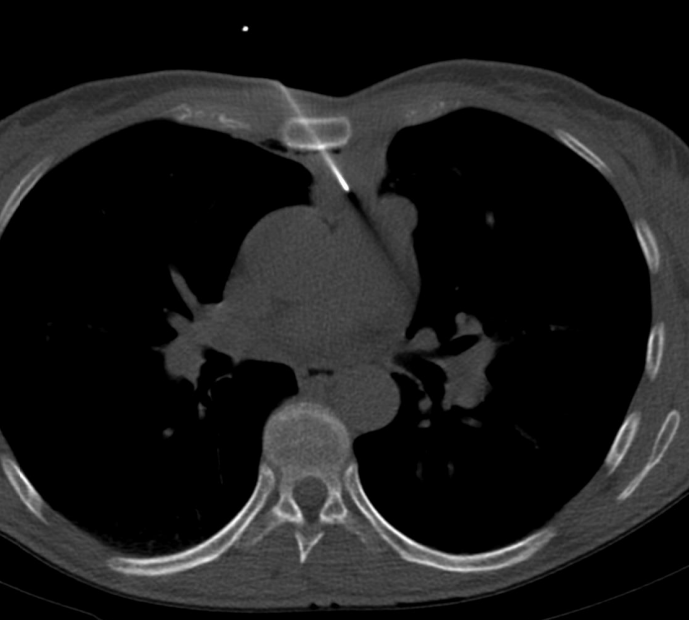
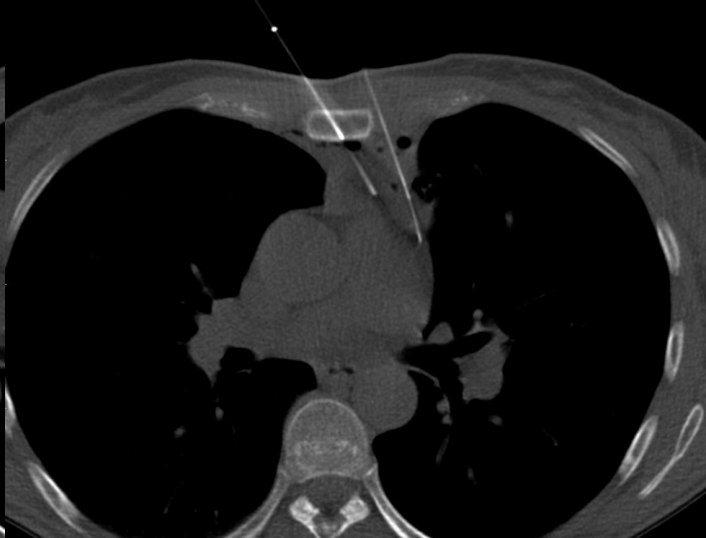
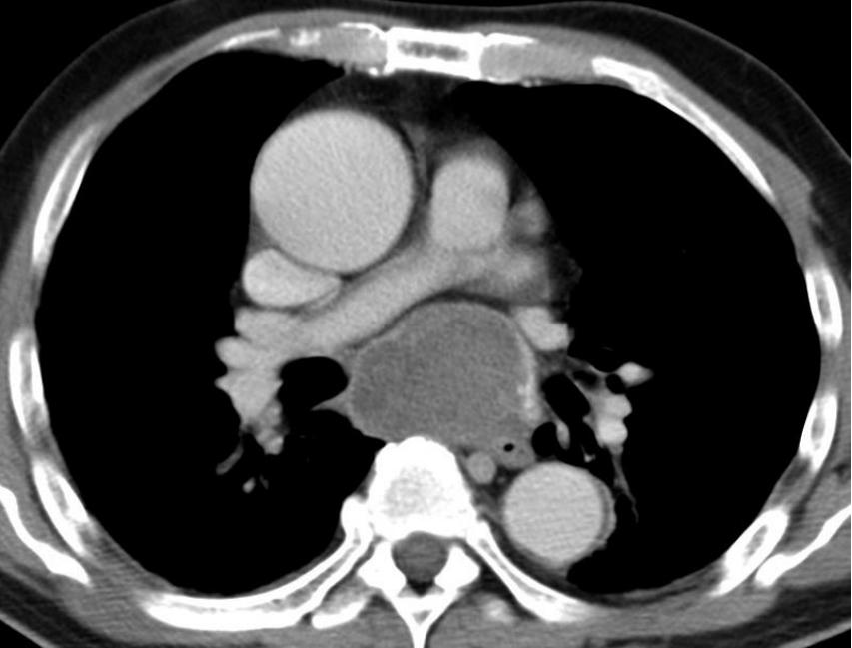
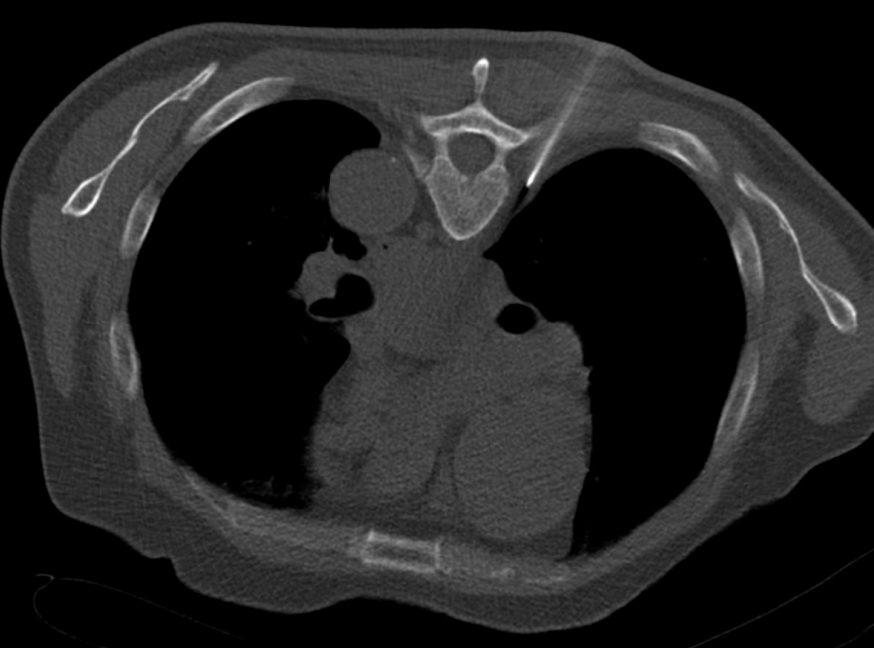
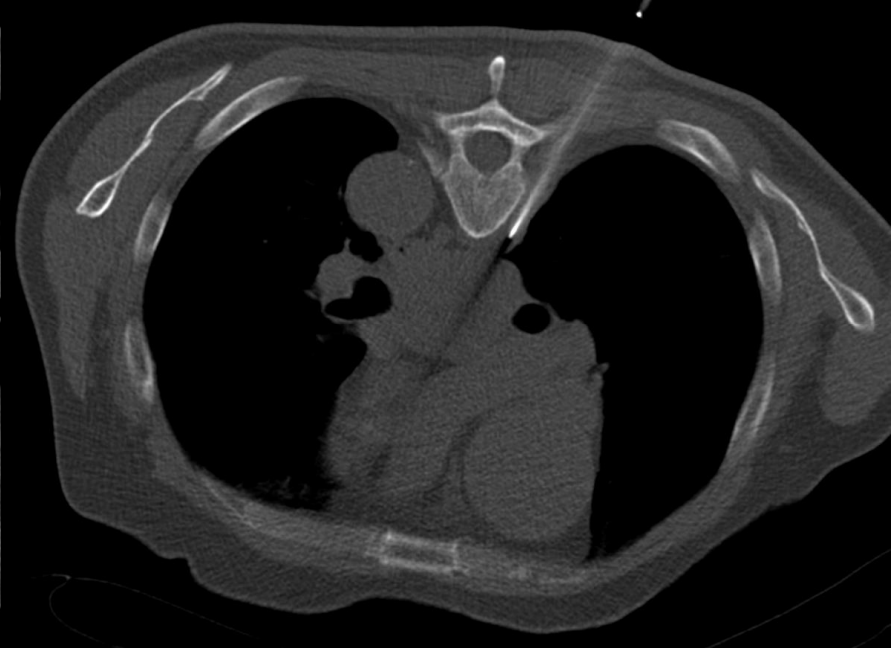
4. 不能诊断的纵膈肿物 Undiagnosed mediastinal mass 纵隔肿块包括各种不同的实体肿瘤,如胸腺/肺恶性肿瘤、淋巴瘤或恶性生殖细胞肿瘤,但也可能是胸骨后甲状腺。在诊断纵隔镜检查前,应对可接近的病变(有安全穿刺路径)病变尝试影像引导活检
年轻患者,上纵膈肿物伴体重下降
5. 靶向治疗进行肿瘤的活检或再活检 Biopsy or re-biopsy of malignancy for targeted therapy
活检以获得足够的组织进行分子病理分析,以确定可接受靶向药物治疗的突变(K-ras、EGFR、EML4-ALK、ROS1)。▪一线治疗后进展的患者可能需要重新活检,以发现可能的新的生物学特征,并指导治疗决策(30%的患者)
特别是对于大肿瘤/治疗肿瘤的患者,PET/CT或CE-CT可能是有利于指导活检
评价患者危险和获益,如果病人包括经济情况或身体状况,即使活检结果也不能继续治疗,应视为禁忌症
安全操作 但可能会出现许多并发症 患者应被告知并表示同意 介入放射科医生: 危险因素取决于患者,肿瘤和手术 个人偏好:考虑替代诊断技术和临床耐受性
肺病变,明显增生 持续性灶性浸润,病因不明。 周围型肺肿瘤,可能不适合通过内窥镜方法进行活检 PNB的适应证和部位:多学科共识
获取肿瘤样本进行免疫组织化学、分子分析:选择个性化的靶向治疗 Yoon SH et al. 2020 clinical practise guideline for PNB of pulmonary lesions. KJR 2021 Veltri A et al CIRSE guidelines on percutaneous needle biopsy CVIR 2017
1) A new or enlarging solitary nodule or mass
2) Multiple nodules in a patient without known cancer or in prolonged remission
3) Focal parenchymal infiltrates in which an infectious organism cannot be isolated
4) Diagnosis of hilar masses following negative broncoscopy
5) Undiagnosed mediastinal mass
6) Biopsy or re-biopsy of malignancy for targeted therapy
Anzidei et al. Insights Imaging 201 |


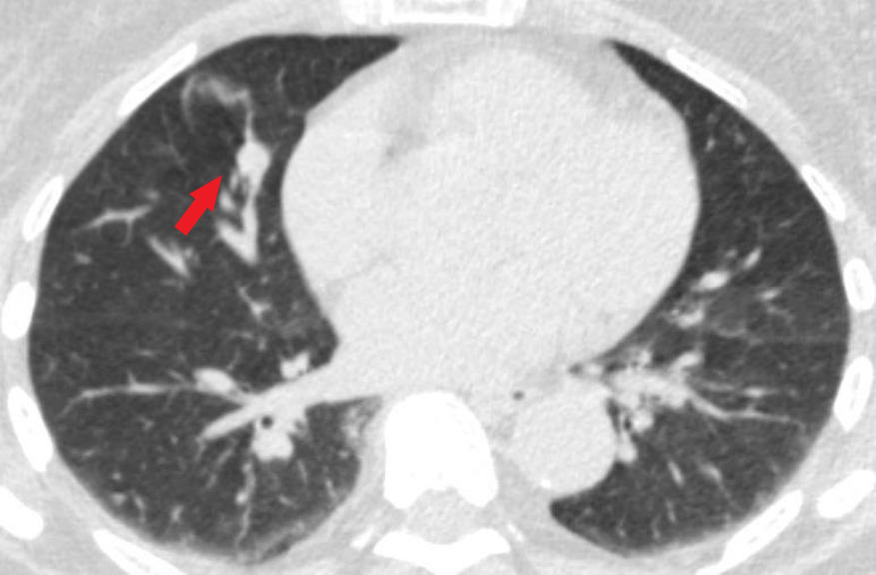
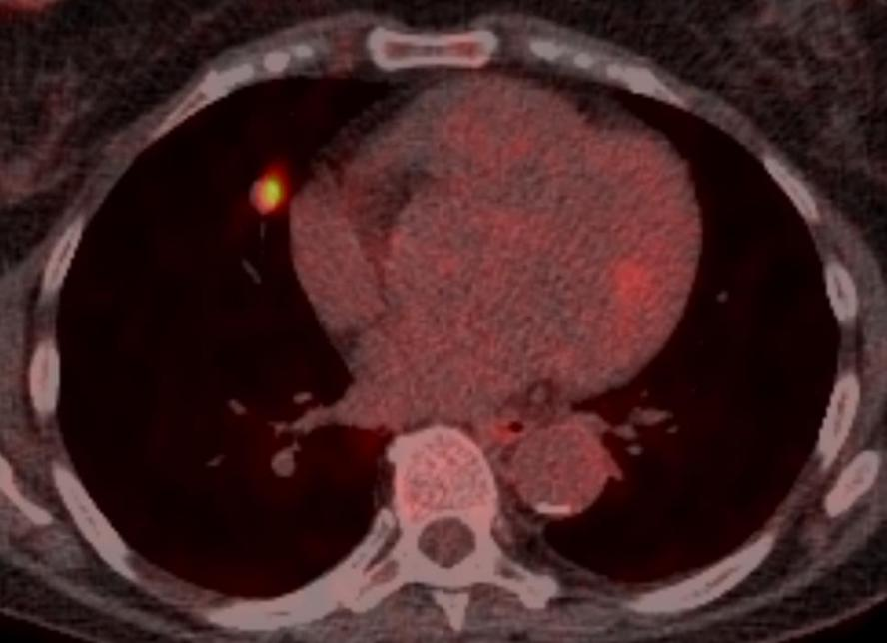
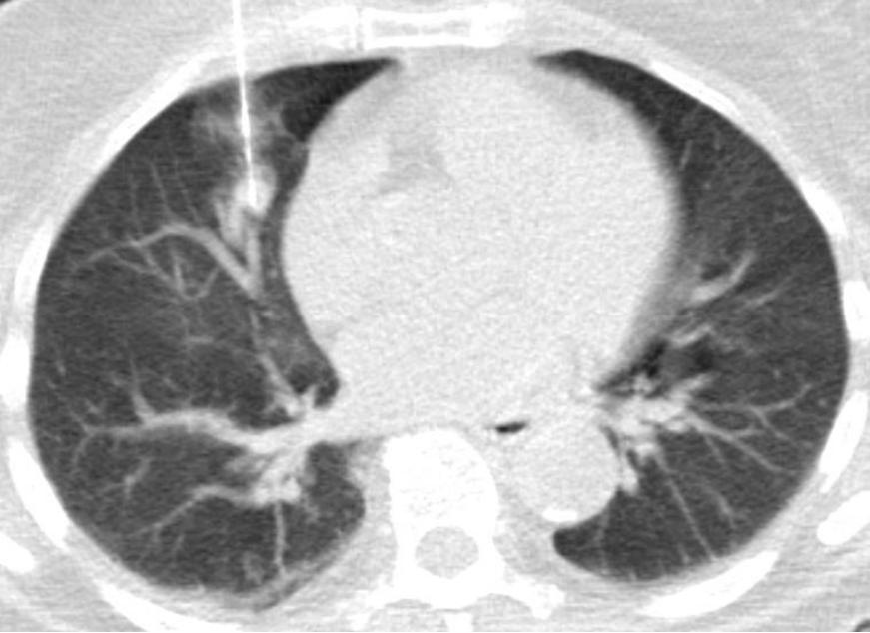
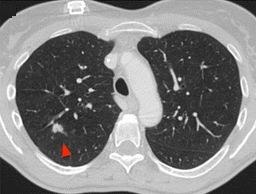
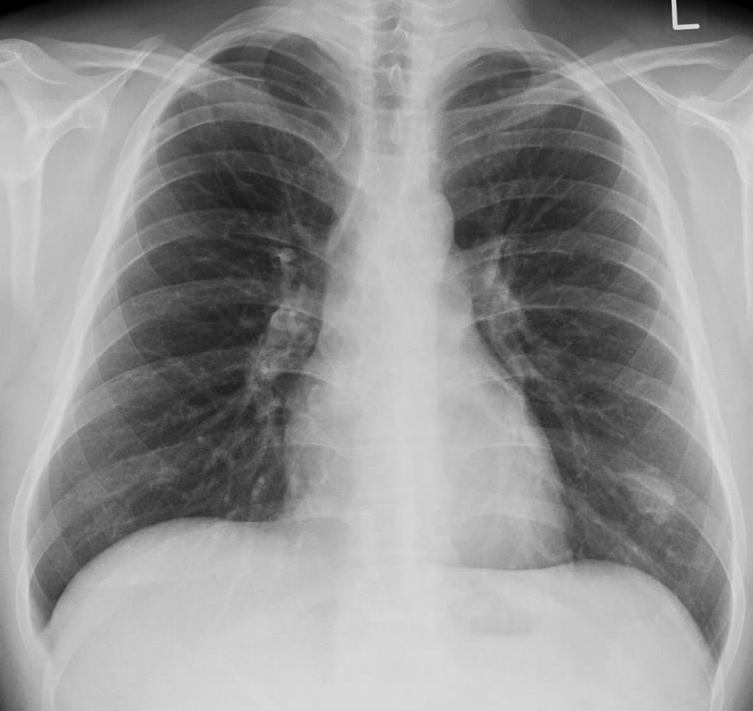
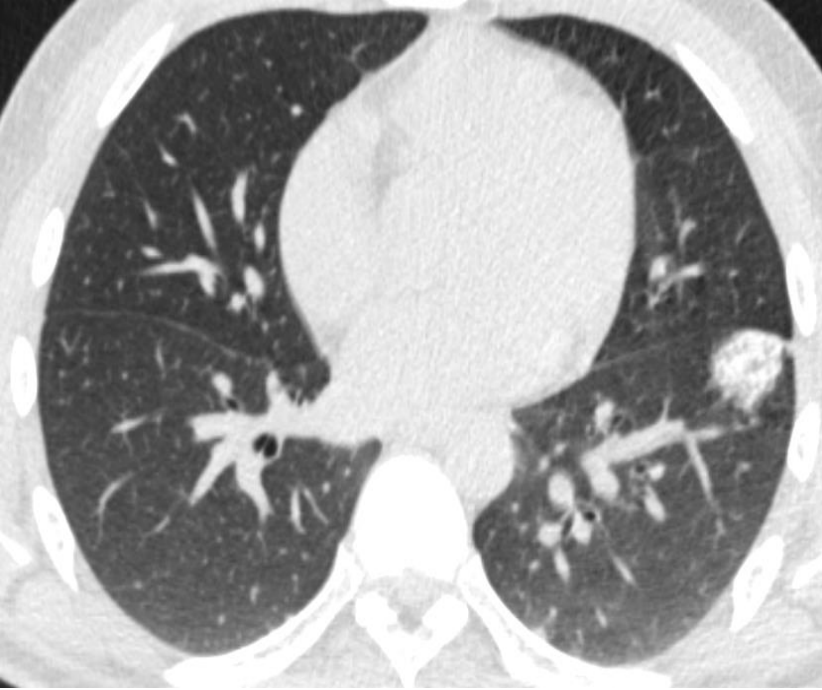
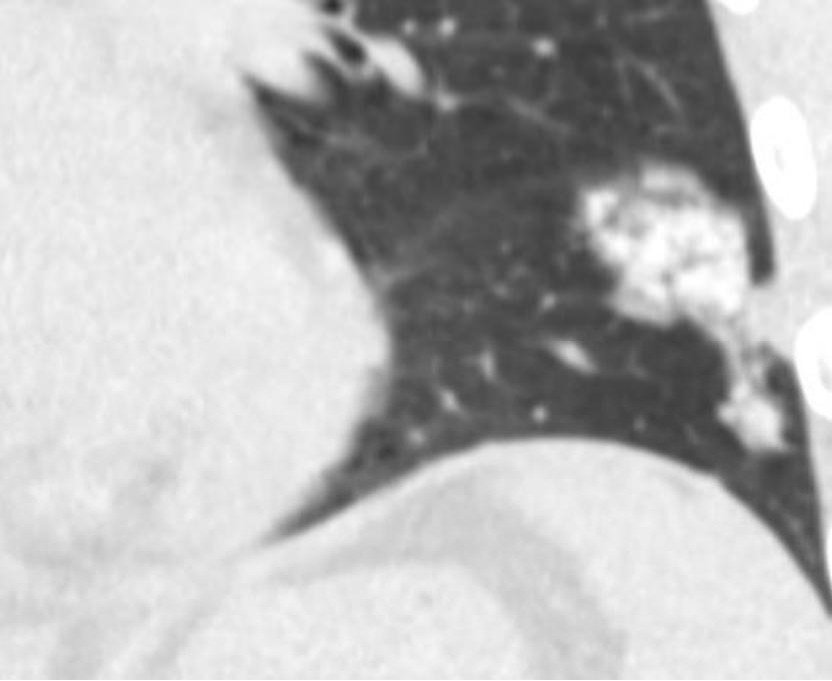
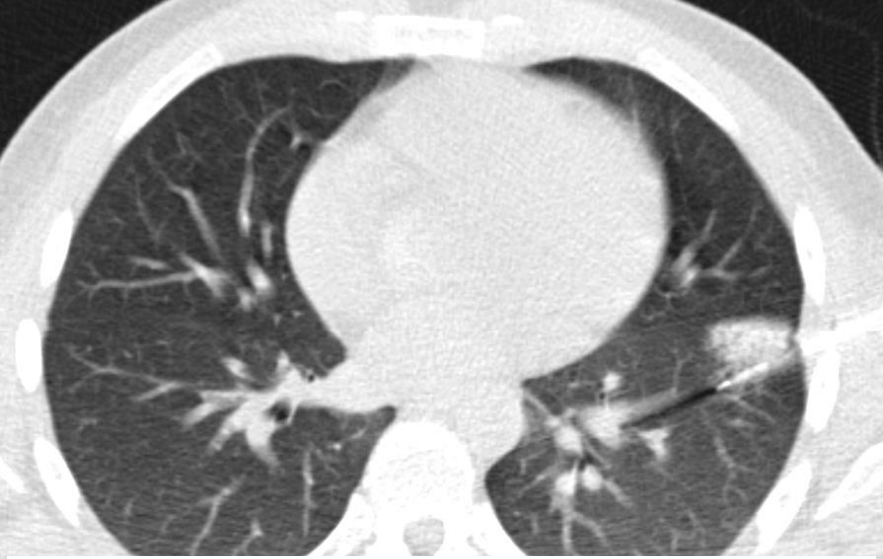
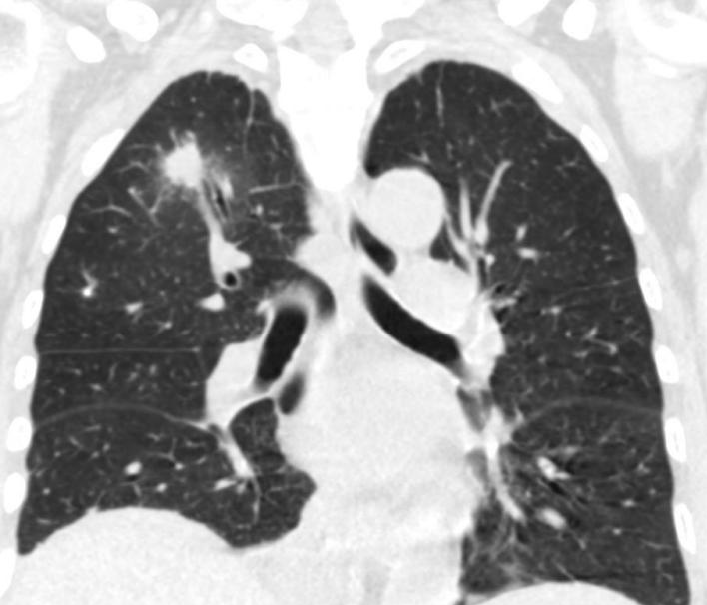
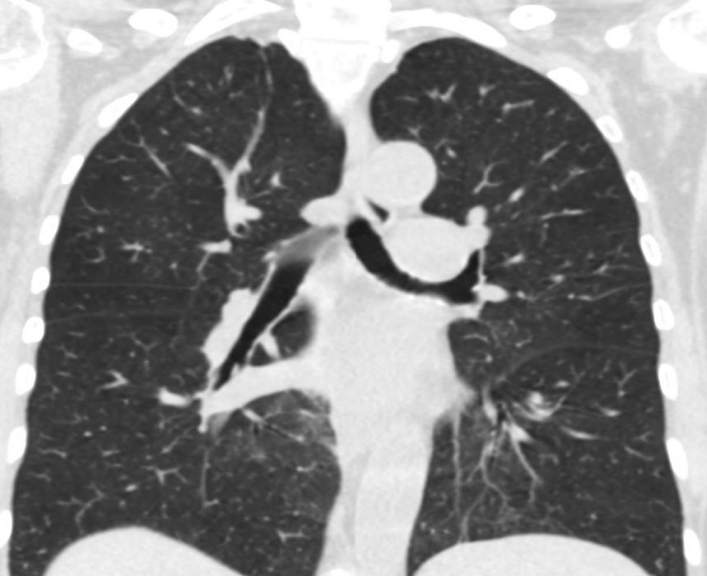
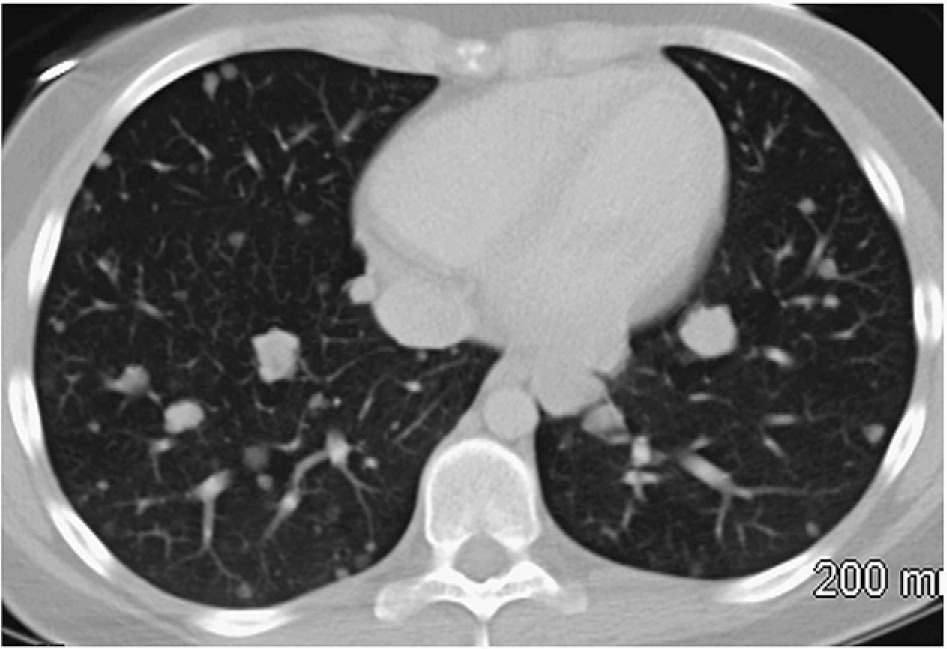
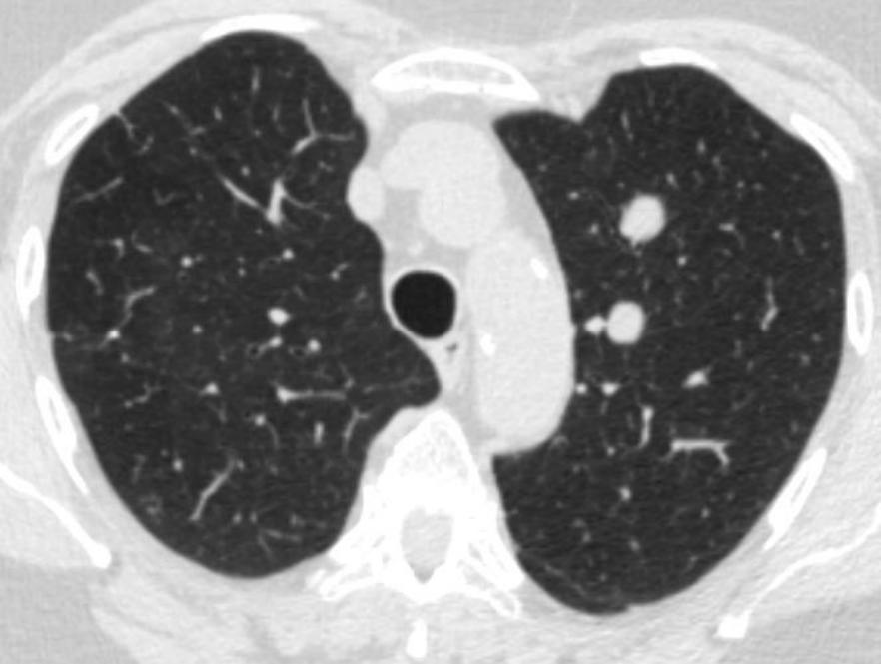
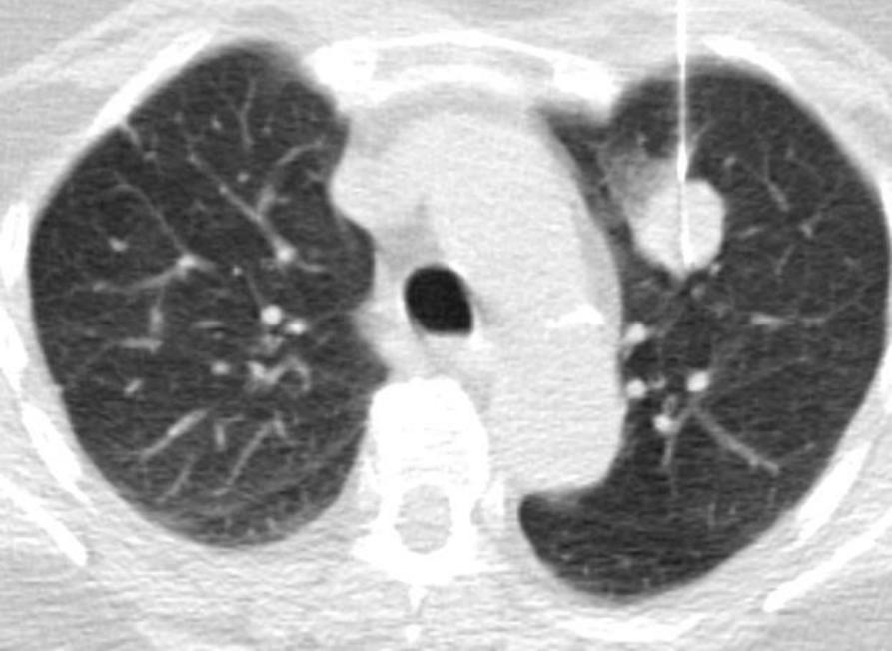
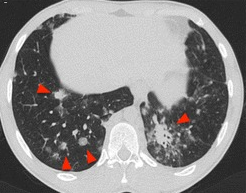 有一种肺活检的适应症叫做不是肿瘤
有一种肺活检的适应症叫做不是肿瘤