非小细胞肺癌(NSCLC)占所有肺癌的85%,是全球癌症死亡的主要原因之一,带来了显著的治疗挑战。对于早期NSCLC,肺叶切除术和淋巴结切除术仍然是推荐的标准治疗方法。尽管开发了亚肺叶切除术(SLR)以限制肺叶切除术的功能损害,但大约三分之一的患者因医学共病、表现状态差和/或肺功能差而不适合手术。
对于这些“非手术”患者,立体定向体放射治疗(SBRT)已经取代了常规放射治疗,并已成为手术切除的主要局部治疗替代方案,使得5年总生存率约为42-55%,局部控制率为85-93%。
经皮热消融(TA)自20年前首次发表介绍这种方法以来,在世界各地的许多中心越来越多地用于早期NSCLC的治疗。作为一种独立的技术,TA在同一次会话中提供了活检和治疗的优势;多学科讨论有助于根据每个病例指导管理。起初,仅限于使用射频消融,现在市场上有不同消融系统,采用不同的消融方式,例如微波和冷冻消融。本文将回顾经皮TA及其不同消融方式在早期NSCLC治疗中的作用和证据。
经皮热消融(TA)自20年前首次发表介绍这种方法以来,在世界各地的许多中心越来越多地被使用和实践,用于早期非小细胞肺癌(NSCLC)的治疗。作为一种独立的技术,TA在同一次会话中提供了活检和治疗的优势;多学科讨论有助于指导每个病例的管理。最初,仅限于使用射频消融,现在市场上有不同消融系统的不同消融方式,例如,微波和冷冻消融。本文将回顾经皮TA及其不同消融方式在早期NSCLC治疗中的作用和证据。
早期肺癌的消融治疗是一种微创的局部治疗手段,尤其适用于无法耐受手术或拒绝手术的患者。它通过物理或化学方式直接破坏肿瘤组织,具有创伤小、恢复快的特点。以下是消融治疗的详细解析: 一、消融治疗的适用人群主要适应症肿瘤特征:
肿瘤直径≤3 cm(部分研究支持≤5 cm,但疗效可能下降)。
位于肺外周(远离大血管、支气管等关键结构)。
患者条件:
心肺功能差、高龄、合并多种基础疾病无法耐受手术或麻醉。
多原发肺癌需保留肺功能(如既往已切除肺叶)。
患者拒绝手术或放疗。
禁忌症
肿瘤靠近大血管、主支气管或纵隔,易造成严重并发症(如大出血、支气管瘘)。
凝血功能障碍或严重肺气肿(增加气胸风险)。
二、常用消融技术及操作流程射频消融(RFA)
原理:通过高频电流产生高温(60-100℃)使肿瘤细胞凝固性坏死。
操作:CT引导下经皮穿刺,将电极针插入肿瘤中心,释放热能。
优势:应用最广泛,技术成熟。
微波消融(MWA)
原理:利用微波电磁场使水分子高速振动产热(可达120℃以上)。
特点:消融范围更大、速度更快,受血流散热影响较小。
冷冻消融(Cryoablation)
原理:氩气快速降温至-140℃,形成冰球破坏肿瘤细胞。
优势:疼痛较轻,可实时监测冰球范围,适合贴近胸膜的肿瘤。
不可逆电穿孔(IRE,纳米刀)
原理:高压电脉冲破坏细胞膜结构,保留血管/胆管等结构。
适用:贴近大血管或气管的肿瘤(研究阶段,需更多证据)。
操作流程:
术前:增强CT评估肿瘤位置及血供,制定穿刺路径。
术中:局部麻醉+镇静,影像实时引导下穿刺,激活能量源消融。
术后:观察4-6小时,无并发症即可出院。
三、疗效与局限性局部控制率
肿瘤≤2 cm:1年局部控制率约85%-95%,3年约70%-80%。
肿瘤3-5 cm:局部复发风险显著升高(需联合其他治疗)。
生存率
Ⅰ期患者5年生存率:约50%-70%(低于手术/SBRT,但高于传统放疗)。
与手术对比:一项Meta分析显示,手术的5年生存率比消融高10%-15%。
局限性
|
| 指标 | 消融治疗 | 手术(肺叶切除) | SBRT(立体定向放疗) |
| 创伤性 | 最小(经皮穿刺) | 大(需开胸或胸腔镜) | 无创 |
| 住院时间 | 1-2天 | 5-7天 | 无需住院(门诊完成) |
| 局部控制率 | 较高(小肿瘤) | 最高(>90%) | 与手术相当(>90%) |
| 肺功能影响 | 几乎无 | 显著(切除肺叶) | 无 |
| 适应症 | 外周小肿瘤、不耐受手术 | 可耐受手术的Ⅰ-Ⅱ期患者 | 不宜手术的早期肺癌 |
选择建议:
优先手术:若患者体能状态良好,手术仍是治愈率最高的选择。
消融/SBRT权衡:
中央型肿瘤或靠近关键结构→ SBRT更安全。
外周小肿瘤、需快速恢复→ 消融可能更优。
六、前沿进展与研究方向
联合治疗提升疗效
消融+免疫治疗(如PD-1抑制剂):利用消融释放肿瘤抗原,增强全身抗肿瘤免疫。
消融+靶向治疗:针对驱动基因突变(如EGFR)患者,减少远处转移风险。
技术改进
多针联合消融:扩大消融范围,适用于3-5 cm肿瘤。
人工智能导航:提高穿刺精度,减少并发症。
扩大适应症探索
部分研究尝试消融用于多原发肺癌或肺转移瘤(需个体化评估)。
七、患者注意事项
严格随访:术后每3-6个月复查胸部CT,监测局部复发或新发病灶。
多学科评估:由胸外科、肿瘤科、介入科共同制定方案,避免单一治疗局限。
功能锻炼:术后呼吸训练(如腹式呼吸)促进肺功能恢复。
总结
消融治疗为早期肺癌提供了重要的“非手术”选择,尤其适合高龄、肺功能差的患者。其优势在于微创、快速恢复,但需严格筛选病例(小肿瘤、外周型)。对于追求更高治愈率的患者,手术或SBRT仍是优先选项。未来随着联合治疗和技术的进步,消融可能在早期肺癌中扮演更重要的角色。
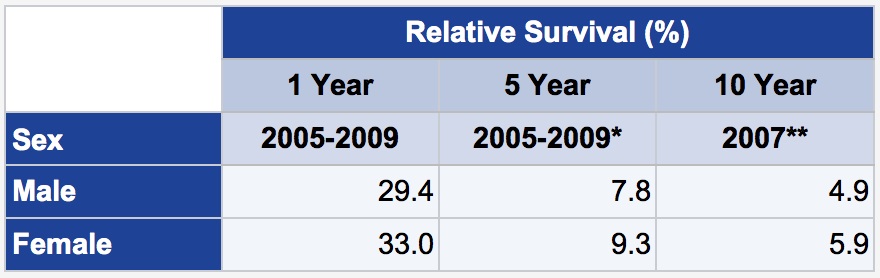
原发肺癌是癌相关死亡最常见的原因之一。(www.cancerresearchuk.org)
肺癌的诊断陷入两难的境地,我们应该筛查吗?尽管可以减少肺癌死亡率将近20%,但从花费效益(Cost-Effectiveness)说,陡升至169000/QALY*。原发性肺癌的治疗面临挑战。
*质量调整寿命年(QALYs, Quality-adjusted life years)- 寿命长,也要有质量;健康的概念已经从传统生物学指标→疾病指标→生存指标→QALY(现在)。政府保健支出的首要目标是创造健康(生存期和生存质量的函数)。
局部消融在肝脏原发和转移癌方面已经达到令人印象深刻的结果,不管是技术上,肿瘤学上还是经济上【de Baere
消融的模式包括两种,热消融和冷冻消融。
(1)热消融
- 射频消融(RFA):该技术的原理是在CT 、彩色B超的引导下,将多极子母针消融电极准确刺入肿瘤部位,射频消融仪在电子计算机控制下将射频脉冲能量通过多极针传导到肿瘤组织中,使肿瘤组织产生局部高温(70 ℃ -95 ℃),从而达到使肿瘤组织及其邻近的可能被扩散的组织凝固坏死的目的,坏死组织在原位被机化或吸收。
- 微波消融(MWA):微波介入指的是利用频率900MHZ(包含900MHZ)的设备用电磁方法引起肿瘤组织的破坏口。在微波消融中主要依靠偶极分子的旋转来产生热量。水分子是偶极分子并且有不平衡的电荷分布,在微波震荡电场中通过水分子的剧烈运动摩擦生热而导致细胞凝固坏死。当前微波消融术主要用915MHZ和2450MHZ两种频率(百度)。
- 可控地破坏局部活性组织的治疗方法。将组织快速冷冻,温度降到0℃以下,细胞内、外的组织液形成冰晶,细胞结构被破坏。继之细胞脱水,膜系统的脂蛋白变性,组织发生缺血性梗塞,营养缺乏,而终至坏死。
肺癌消融学习的目的是了解原发性肺癌局部消融的适应症和禁忌症(包括综合治疗的概念)。恰当地评价局部消融和其它治疗潜在的不同;了解消融治疗的一些特殊的限制以及消融后潜在的并发症;熟悉原发肺癌消融后短期和长期结果。

