远端脑保护装置有两种,远端球囊阻塞装置和远端虑伞装置
尽管有了细致的技术和成熟的经验,栓塞性卒中仍然是颈动脉支架置入(CAS)的一个主要障碍。绝大多数这种神经系统并发症都是由不同操作阶段中的斑块碎片或血栓造成颅内栓塞导致的。抗栓塞装置降低CAS中栓塞事件的发生率已经在国内外广泛应用。目前已经前瞻性地对使用远端堵塞球囊保护(GuardWire 系统, PercuSurge-Medtronic, Mineapolis, MN)下的CAS结果进行了检验,来评价这种治疗方法是否可以同颈动脉内膜剥脱术或没有抗栓子保护的CAS的历史对照相比较。
 PercuSurge GuardWire系统 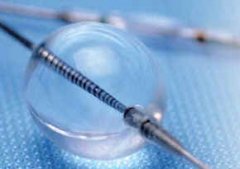 PercuSurge GuardWire 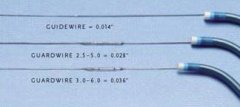 安装在GuardWire临时堵塞导管上的外向抽吸导管 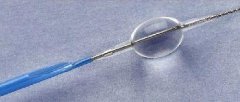 PercuSurge GUARDWIRETM 技术方法
经股动脉入路首先将一根7F多用导管或一根6F长导引鞘管(取决于支架种类)放入颈总动脉(CCA)中。然后顺着导引导管轻轻地将GuardWire送向前,穿过病变部位,将保护球囊的标志放在病变部位远端2或3cm。然后接上微封口接合器,用固定体积的稀释造影剂缓缓地使保护球囊充盈,堵塞ICA,使血流逆转入颈外动脉(ECA)。注射造影剂确认ICA内的血流已经被完全阻断是很重要的,这样才能保证在操作过程进行充分地脑保护。如果ICA的直径较大,建议将保护球囊放在ICA高处颅底的位置,在那个节段ICA直径要小一些,这样就可以达到球囊的稳定。在松开微封口接合器时,球囊保持充气状态。然后在保护下进行病变处的预扩张或直接支架置入。产生的所有碎片都通过单纯的抽吸或抽吸联合冲洗技术从ICA内移出。使用了两种保护技术:
技术1:堵塞球囊在整个操作过程中都保持充气状态,在完成支架置入和后扩张后进行一次抽吸。 技术2:在预扩张和支架置入之间,使堵塞球囊放气恢复脑血流。在这两个步骤之后都要进行抽吸。 使用什么样的技术取决于病人对堵塞的耐受力,大脑侧支循环,对侧动脉的状态,操作的持续时间,以及遇到的技术问题。在这两种情况下,都是顺着导丝将抽吸导管向前伸进入扩张的区域,用一个与之连接的20cc注射器抽吸出碎片。至少要进行2次成功的抽吸。 另外,也可以从导引导管注射入生理盐水冲洗治疗的区域,将颗粒冲向ECA。用一个注射器以2ml每秒的速度注射10秒钟。可以进行2次冲洗:第一次将导引导管放在颈动脉分叉处,第二次将导管放在保护球囊附近。如果只可能进行一次冲洗,建议将导引导管头端放在堵塞球囊附近。最后,将微封口接合器从GuardWire上撤下,使堵塞球囊放气,恢复正常血流。如果血管造影的结果满意,就可以将装置撤出了。
临床试验资料
在1998年2月至2002年2月之间,有238名病人(264处颈动脉狭窄)符合入选标准,并且进行了GuardWire脑保护系统下的CAS。根据北美有症状颈动脉内膜剥脱术试验(NASCET)标准,经血管造影评价颈内动脉(ICA)狭窄等于或大于70%直径的病人符合治疗条件。 以下病人被从治疗范围中排除:ICA有多处狭窄,颅内病变,血管造影显示有血栓,在最近的6个月内出现过消化道出血,出血性疾病。
所有病人都必须终生服用阿司匹林每天75至300mg,最好在操作前1周,至少2天,以及在操作后1个月内,应该每天服用噻氯吡啶250至500mg或氯吡格雷 75mg。在导引鞘管放置后,常规使用普通肝素(5000IU 静脉使用)和阿托品(1mg 静脉使用)。病人通常在操作当天就出院。 在进行CAS的前一天,所有病人都要进行神经系统检查,超声扫描,和计算机体层成像(CT)扫描,在操作后第30天以及此后每6个月都要进行神经系统检查和超声扫描,在操作后第6个月要进行一次血管造影。在CAS后神经系统状态发生任何改变都应该重复CT脑扫描。通过以下终点事件来进行对GuardWire系统的评价: 主要临床终点包括操作后第一个30天内发生的任何重度/轻度卒中,死亡,或心肌梗死(MI)。围操作期并发症被定义为在最初的48小时内发生的任何重度/轻度卒中,死亡或MI。次要临床终点包括在6个月以内需要进行再次治疗,血管成形术,或内膜剥脱术。 血管造影的终点为:血管造影成功率,定义为残余狭窄小于或等于30%,和血管造影再狭窄,定义为动脉管腔直径减少大于或等于50%。操作成功被定义为狭窄被减少至小于或等于30%,并且没有发生任何神经系统并发症,MI,或死亡。 238名连续的病人进行了264次颈动脉血管成形术(其中有190名男性,48名女性,平均年龄71.2±9.4岁,范围在40-91岁)。有26名病人进行了双侧操作。有95处狭窄都是没有症状的(36%),169处是有症状的(64%)。共有224处病变是动脉粥样硬化性的,有30处是再狭窄(手术后:27,血管成形后:3),还有8处是放射后狭窄。有一例病变是炎症性动脉炎,还有一例是创伤后动脉瘤。狭窄的平均百分数是82.3±9.2%(70-99)。平均病变长度为14.4±6.3mm(5-50)以及平均动脉直径为5.0±1.3mm(4—7.1);118处(45%)病变有钙化,188处病变有溃疡( 72%)。 使用持续堵塞技术治疗了共216处病变。平均堵塞时间(秒):375±182( 范围141-1480)。 使用两段堵塞技术治疗了共46处病变。平均扩张堵塞时间(秒):320±150( 范围109-765),平均支架置入狭窄时间(秒):300±140( 范围120-720)。全部病变的平均堵塞时间(秒):410±220( 范围120-1480) 。
技术成功率
在264次操作中,有262(99.2%)次取得了技术成功。有两例病例无法用GuardWire系统通过病变部位,原因是狭窄处有非常牢固的钙化,并且CCA和ICA 过度扭曲。在没有大脑保护的情况下成功完成了这两例操作。在一名病人中,完成操作后,无法用微封口接合器使堵塞球囊放气,原因是微封口结合处出现了绞结。用剪刀剪断GuardWire上微封口区远端部分,问题就得到了解决,球囊立即被放气。在10名病人中观察到堵塞球囊部位出现了轻度痉挛,但没有明显的血流减少。没有发现重度痉挛或动脉壁夹层的情况。置入了128个Palmaz支架(P204:73,P154:53,Corinthian:2),36个Wallstent支架,101个镍钛合金自膨式支架,以及一个带膜支架治疗血管瘤。镍钛合金以及Wallstent 支架覆盖了分叉处,但没有损害ECA内的血流。所有支架都展开得很好。
球囊阻塞的耐受性
在进行操作之前,必须对主动脉上的4根血管进行充分的血管造影评价,以确定有来自Willis环,椎基底动脉,和对侧颈动脉的充分的侧支循环。这些结构有先天缺如或有获得性疾病的病人可能无法耐受球囊阻塞时血流中断。这个问题同颈动脉内膜剥脱术中的手术钳夹相似但不完全相同,因为在使用堵塞性球囊时,ECA中的血流不受影响。这根血管同样也为大脑的前循环和后循环提供了侧支血流,这在ICA堵塞时是有用的,但在用冲洗清理治疗区域时可能是有害的。在一研究中,绝大多数的病例都能良好地耐受ICA堵塞。有4.2%(11例)不耐受的病人。但只有更少病例(2例)是完全的严重不耐受(在血液中断后立即出现症状)。 更为常见的情况是,在操作已经开始后,出现延迟的短暂的不耐受,常常在支架展开后,进行碎片抽吸前。在这些病例中,可以在进行抽吸后完成操作,然后重建大脑血流,这样就能保持保护的益处。尽管有病人有严重的对侧ICA狭窄,或有对侧ICA堵塞,应该重视少数无法耐受的病人。Mehran等人报告了8%的不耐受率。共有251例都能很好地耐受保护球囊充气期间的堵塞,其中62名病人有严重的对侧ICA疾病(狭窄或堵塞)。观察到两种类型的不耐受: 1. 有两名病人( 0.8%) 在堵塞球囊刚刚充气后完全无法耐受:有一名病人对侧ICA完全堵塞,球囊充气后出现意识丧失和抽搐。在快速将球囊放气后,病人完全恢复了。在没有抗栓塞保护的情况下成功地完成了CAS。有一名病人Willis环的侧支循环发育不良,球囊充气后很快出现了意识丧失,但可以在有保护的情况下完成操作。在球囊放气后,这名病人很快恢复了。 2. 部分性一过性不耐受(有9名病人出现:3.4%),即约在血流中断2分钟后出现一过性症状,例如躁动,短暂的意识丧失,或一过性的神经功能缺陷。可以在有保护的情况下完成操作。所有的病人在保护球囊仍保持充气的状态下很快完全恢复。其中有7名病人对扩张出现了低血压反应,出现心动过缓,这可能促进了不耐受的发生。有10名病人出现了扩张区域以上保护性球囊位置处的ICA痉挛,但通过血管扩张剂治疗很快好转。 碎屑的收集
所有病人中都进行了碎片的抽吸。抽吸得到的血样被收集在滤器(孔径为40um)中,通过光学或电子显微镜技术对其进行分析。所有血样中都提取出了肉眼可见的碎片[平均直径:250um(范围56—2652),每次操作的平均碎片数量:74(范围7—145)]。发现了不同种类的颗粒:动脉粥样硬化性斑块,胆固醇结晶,钙化结晶,坏死物质核心,纤维蛋白,新鲜和陈旧的血栓,血小板,巨噬泡沫细胞,脂质,以及非细胞物质。 并发症
1. 出现了5例(1.9%)神经系统并发症,包括: (a)4例围操作期并发症(1.5%): 在一名右ICA狭窄伴溃疡的病人中,操作中出现Wallstent急性血栓形成后发生了单眼黑蒙。在堵塞球囊放气后通过血管造影发现了血栓。快速重新使球囊充气并且注射了阿昔单抗(静脉使用冲击剂量每千克0.25mg,此后12小时连续输入10ug/kg)。10分钟后通过导引导管进行了血栓抽吸和冲洗,然后保护球囊最终被放气。最后的血管造影显示支架内没有残余血栓。然而,病人出现了黑蒙,可能是ECA内的栓子通过ECA-眼动脉交通进入的结果。事实上,在对血管造影图像进行仔细检查后确实发现了一根ECA和眼动脉之间的交通支。
总共发生了3例短暂性脑缺血发作(TIAs):在对一名无症状的左ICA狭窄的病人进行CAS后,出现了TIA伴一过性的轻偏瘫,这名病人的堵塞时间延长(19分钟)。在后续的系列CT检查中,没有发现缺血的证据。 发生了两例TIA伴上肢单瘫,在CT扫描检查上没有发现缺血征象。 (b)在一名无症状右ICA不全性堵塞的病人中,在CAS操作后第3天,使用阿昔单抗( 同上述方案相同)的情况下,出现了脑出血伴偏瘫。这名病人在2个月后部分恢复了。
2. 心脏事件(0.4%): 一名有症状的病人在进行CAS操作3周后死于心力衰竭。在住院期间或CAS后30天内,没有发生心梗。
3. 30天内神经系统并发症以及死亡的发生率共为2.5%(黑蒙:0.8%,TIA:1.3%,死亡,0.4%)。 4. 没有发生脑神经麻痹。
随访
在平均23±12个月(范围1—46个月)的随访期内,出现了4例死亡:有一名病人在第6个月死于重度卒中,卒中定位在先前治疗的ICA对侧的大脑半球,另有两名病人死于心肌梗死,有一名病人死于癌症。在随访期内没有发生轻度或重度卒中。在第6个月时,观察到一例无症状的在狭窄,经球囊血管成形术成功地对其进行了治疗。在第36个月时,没有发生事件的存活率为97%。 临床和技术提示
体外人颈动脉支架置入技术已经显示了碎片迁移和远端栓塞的频率,并进一步得到了临床研究的证实。经皮技术产生的栓塞性颗粒数目似乎比内膜剥脱术产生的要多。其临床重要性正在得到证实,这些栓子的存在不可能对大脑有任何益处。另外,能够引起缺血事件的最小栓子大小现在还未得到确定。有人建议将不同的病人及斑块特性作为产生碎片和栓塞性事件的预测因子,来确定CAS操作的高危人群。在研究中从所有病人处取得了碎片,即使是理论上认为发生脑梗塞风险较低的病变(再狭窄,有回声斑块,中心性病变),结果提示栓塞的风险同斑块性质无关。另外,支架展开并不能为栓塞性斑块碎片迁移提供充分地保护。在所有的CAS系列中,无论采取什么样的置入技术或支架有何种特性,都存在栓塞的风险。Manninen等人在尸体原位中比较了颈动脉血管内支架置入和经皮经腔血管成形术(PTA),发现在远端栓塞方面两者没有区别。 1984年,Vitek等人首次报告了一例无名动脉血管成形术的成功病例,当时用一个次级球囊导管暂时堵塞了右CCA的开口处,降低了脑栓塞的风险。在最近的10年内,由于血管成形术的不太完美的结果以及排除栓塞风险的需要,已经设计出了数种CAS中的抗栓塞策略。 Oesterle等人首次在动物身上对GuardWire系统进行了测试,接着在27例冠状动脉大隐静脉移植物的操作中进行了临床使用。结果显示,该系统可以适配用于常规的血管成形术操作,能够容纳并且抽吸出动脉粥样硬化碎片,并且可能帮助预防远端栓塞。主张将该装置用于CAS中的脑保护。它的优点之一在于,它操作起来很像容易控制的冠状动脉导丝,能够轻松地穿过狭窄部位,减少技术失误。报告中有238名病人(264处颈动脉狭窄)符合入选标准,并且进行了GuardWire脑保护系统下的CAS只有2次(0.8%)不能将其穿过扭曲的CCA和ICA中的牢固钙化狭窄处。在绝大多数病例中,抗栓塞装置都能在支架置入前放置好。不建议在支架置入后放置保护装置来预防更高的栓塞风险。 对于无法穿过病变部位的病例,可以在置入保护球囊之前用一个小的冠状动脉球囊进行一次预扩张,以帮助GuardWire通过。另外,GuardWire 提供了足够的支持帮助将扩张球囊和支架送向前。堵塞球囊的放气事件很短,持续约15秒。 技术限制
联合远端堵塞脑保护装置的CAS是一种可行而且安全的操作,30天内的神经系统并发症发生率非常低(1.9%)。在同没有保护技术的系列以及历史手术对照进行对比时,结果是令人满意的。Roubin等发表了从一个单中心实验中获得的有利结果。在一个系列中,进行了329例有保护的操作(232例使用了GuardWire),栓塞性事件的发生率为3%。Schlueter等人也显示了这种保护的有效性。在一个进行了103例操作的系列中,有5例(4.9%)围操作期事件,1例轻度卒中,以及4例TIA,但在99名成功置入该装置的病人中,只有3例(3%)TIA发生。在4名置入该装置失败的病人中,2名出现了严重的围操作期神经系统并发症。 但是脑保护无法防止所有的斑块碎片造成栓塞,并且栓塞性事件仍然可能在操作中的任何步骤中发生。堵塞球囊脑保护装置只是在导丝穿过病变部位后提供了抗栓塞保护。而用导丝穿过病变部位的操作,以及最初将导引导管放入CCA中的操作,同样也能释放栓子物质。使用更小的工具以及改用冠状动脉技术可能会限制风险并且产生更好的结果。 Mathias和Jaeger 曾进行了一项非常有趣的研究。他们研究了70例没有脑保护的CAS操作和102例有脑保护(78%使用了GuardWire ,22%使用了AngioGuard 滤器)的CAS操作,在操作中用经颅多普勒(TCD)进行监测,在进行CAS之前和之后24小时进行脑部磁共振成像(MRI)。有了TCD,就可以在颈动脉血管成形术的不同阶段计算病人的微栓子信号(MES)数目。尽管有抗栓塞装置,仍然可以记录到栓子信号,但没有保护的情况下记录到的MES数要多得多,并且对于大脑栓塞而言更为关键的步骤是预扩张,支架置入,以及支架内扩张。通过MRI,Mathias和Jaeger注意到新出现的高信号病变在未进行保护的血管成形术中更为常见(28.5% 相对于8.2%)。 Al-Mubarak等人公布了相似的结果,即没有进行保护治疗的对照组病人中出现的栓子数目更多。在CAS中使用这种抗栓塞策略,血流必须被完全阻断并且逆转入ECA中。各种大小的颗粒都被堵在ICA内。操作者必须清楚应用这项技术时潜在的问题: 1. 在操作中,堵塞球囊可能会放气或可能变得堵塞不完全,有时候只是在收缩期或对狭窄进行扩张后(由于血流改善,血管直径可能增加)。一些颗粒仍然可能迁移至大脑中。因此,在堵塞球囊充气后,进行操作之前,注射一次造影剂确认ICA被完全堵塞是非常重要的。如果阻断ICA内的血流有困难,最好将球囊放置ICA高处颅底部位。 2. 可能有一些颗粒太大而无法抽吸出来(非常罕见)。
3. 在充气的球囊下端存在一个盲区,一些卡在这个区域中的颗粒可能很难或无法用抽吸导管吸出。在球囊放气时,这些颗粒可能会迁移至大脑内。在这种情况下,用抽吸导管注射生理盐水冲洗这一区域可能会对清理这个盲区有帮助。
4. 在球囊堵塞ICA期间,血流被逆转至ECA中,这样就有可能通过大的侧支(至大脑中动脉或椎动脉)造成脑栓塞和视网膜栓塞。侧支循环通过眼动脉,咽升动脉,上颌内动脉存在于ECA和ICA之间,通过枕动脉和咽升动脉存在于ECA和椎动脉之间。因此必须非常清楚这些侧支循环造成的脑栓塞风险,并且在开始操作之前进行一次好的脑血管造影确认这些侧支循环是很重要的,在这种情况下,就应该采取一种不同的保护策略(滤器或逆转血流)。最近Al-Mubarak等人对这一并发症进行了小心地描述。
脑保护不能预防晚期栓塞现象。约有30%的晚期TIA发生在操作后2至10天的范围内,30%的轻度卒中发生在支架放置后4至10天范围内。这些晚期TIA和轻度卒中可能与斑块移动和/或来自支架支柱之间以及支架附近的血栓有关。这些事件代表了一种延迟的栓塞现象,这一现象最近由Wholey等人在一个472例没有保护的血管成形术系列中描述,同时Qureshi等人以及Mehran等人也对这一现象进行了描述,他们报告了CAFÉ USA试验的结果,这是一个前瞻性多中心登记研究(7个中心)。在这个包括212例操作的系列中,对97%的病例都成功地放置了该装置,仅描述了3例(1.4%)操作期间出现的卒中,显示了GuardWire的有效性。然而,在第一个30天内,发生了3例死亡(1.4%),其中有2例是神经性的,11例(5.2%)轻度卒中,以及5例(2.4%)TIA,但没有出现重度卒中。平均出现神经系统事件的时间为5.0±1.2小时,同其它经验相比大大延迟了。在我们的系列中我们没有观察到这样的晚期神经系统并发症。我们认为用抽吸导管进行细致的抽吸是一个重要的技术点,这样帮助消除血管成形术和支架置入后残留的颗粒,避免神经系统并发症。严格地监测血压和心率也很重要。一些病人有更高的风险:那些高龄和原来有过卒中史的病人,高度狭窄,透回声的斑块。使用糖蛋白(GP)ⅡB/ⅢA抑制剂以及最后测量活化凝血时间(ACT)也是起作用的因素。Ahmadi等人通过他们的包括320例操作的系列指出,学习曲线也起到了重要作用。30天内并发症发生率在最初80名病人中是15%,在其他病人中仅为5%。
脑保护同样也无法预防脑出血,而脑出血可以在操作结束后出现,并且在大多数发表的系列中都有发生。大多数情况下,这是一种灾难性事件,尽管控制了血压也可能出现不良预后,并且可能是由成功进行血管成形术和支架置入后脑血流过度灌注所致。这种综合症被认为是继发于长期灌注压降低的正常脑血流自动调节失败所致。有几个因素可能促成这种过度灌注综合征的发生:大于或等于90%的严重同侧狭窄,由其它颅外血管严重堵塞性疾病或Willis环不完整导致的侧支血液循环受损,围操作期高血压,以及使用抗血小板药物或其它种类的抗凝药。 纤溶药物可能会促进脑出血。尽管它们的成功率处于边缘地带(约40%的病例),在有血管造影证明堵塞的灾难性事件中,纤溶药物仍然是适宜的治疗方法,这种堵塞一般是由大的斑块样的栓子造成的。这些斑块不能被溶栓药物有效溶解,这样就更加需要在颈动脉支架置入过程中使用远端保护装置。 还有一些并发症也可以在使用这些保护装置的情况下出现。可能在放置保护性球囊的地方看见有痉挛发生,用解痉药物就可以很容易地解决这个问题。Castriota等人描述过由于保护性球囊堵塞动脉而造成的ICA夹层。在用非常低的压力对球囊充气的情况下,这种并发症应该非常罕见。
冲洗
在抽吸后,仍然有一些碎片可能残留在治疗区域。通过冲洗清理这一区域,对于存在侧支循环的病人,这一技术可能导致缺血性并发症。必须在治疗之前进行诊断性的血管造影,对这些特殊情况进行诊断,这种情况下提示应该省略冲洗的步骤,仅通过抽吸移除碎片。在有238名病人(264处颈动脉狭窄)GuardWire脑保护系统下的CAS系列中,一例冲洗后出现了神经系统并发症(黑蒙)。在出现这一情况后,作者们放弃了冲洗的操作。在清理操作中以高压过度冲洗可能导致血液逆流至CCA的开口处(对右侧危害更大,因为右侧CCA通常更短)以及/或者逆流至右侧椎动脉,这样就有引起这一区域神经系统功能缺陷的风险。现在认为,对大多数病例,细致地抽吸就足以清理治疗区域。 操作的考虑事项和晚期结果
预先使用阿斯匹林和塞氯吡啶或氯吡格雷进行治疗的重要性,及其治疗时间,在预防并发症中似乎很关键,但作用尚未得到证明。需要进行一项随机试验对这一事项进行严格检查。然而,考虑到这些药物对冠状动脉支架置入的重要性,似乎无需进行这种试验。阿昔单抗已经被建议作为一种辅助治疗。其潜在的益处和适应证还有待评价。有人也认为,只是在操作中发生并发症的情况下才需要使用这种药物。 在随机进入NASCET和无症状颈动脉粥样硬化研究(ACAS)中的一群选择性的低手术风险的病人群体中,结果显示,缓解颈动脉堵塞能够降低脑血管事件的风险。但还不能明确了解在其他有不同基线特征的病人群体中,缓解堵塞是否也会产生这种相同的治疗优势,同样也不了解在预防高危病人的卒中和死亡中,CAS 和CEA的相对有效性。在Shawl 等人的系列中,在19个月的随访期内,病人中发生的神经系统事件非常少,提示缓解堵塞的有效性可能很好地反映为长期临床获益。在Roubin等人的由528名连续的病人组成的系列中,他们描述了3年内没有发生同侧或致死性卒中的幸免率为92±1%,说明颈动脉支架置入可能可以同手术相比较。在大脑保护下进行的CAS系列的结果与之相似并且相当好的远景。 CREST是进行比较CEA和CAS的随机对照试验。已证明CEA有效的病人组中放弃CEA则需要格外小心。有一项比较血管成形术和CEA作用的随机试验,颈动脉及椎动脉经腔血管成形术研究(CAVATAS),已经完成。这项试验,尽管效率不足,提示没有进行常规支架置入的球囊血管成形术同选择性CEA有相似的安全谱。这些数据显示常规支架置入将使这种颈动脉疾病的经皮治疗方法得到进一步改善。Brooks等人也在一项随机试验(104名有症状的病人)中比较了CAS和CEA,并且发现CAS和手术是相当的。 有CEA高风险的病人包括,颈动脉病变位置在C-2或C-3颈椎以上或在CCA开口处的病人,以及有颈椎疾病或颈椎固定的病人,先前有广泛颈动脉手术史,纤维肌肉发育不良,先前颈部放射,以前进行过CEA,以及存在严重合并症的情况,包括不稳定心绞痛,近期MI,和严重的充血性心力衰竭。另外,将会出现不断革新的新型支架,扩张和后扩张策略,以及脑保护装置,这些都需要进行评价。 |

