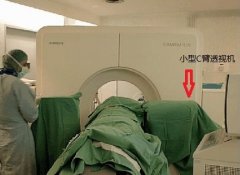
椎体成形术主要基于欧洲和北美的经验发展出了不同的技术。文献中关于操作步骤的描述有很多,但这些技术之间的差异基本上很小并且与产品和器械的有效性以及操作者的训练和个人风格有关。 降低并发症最重要的因素是看见针进入椎体和骨水泥注射到椎体时扩散的情况[2]。已经描述了的技术包括使用标准X线透视引导、CT引导或者CT+透视引导下进行在椎体内穿刺,透视可以是单向,也可以是双向。不管穿刺针的类型,骨水泥的注射液(骨水泥)应始终能在透视观察到其向两侧和前后方分布情况。手术者应当争取使用可用的最高质量的透视,带有多种放大水平和小焦距的功能。双平面数字血管造影术设备的使用是理想的;双平面监测的X线透视图像降低了操作时间并能够直观地看到丙烯酸的注射。但是,单独的一个高质量的单面的设备及颈足够了。避免使用低质量的模拟X线透视便携式设备,因为图像质量通常太差了以至于不够看清骨界标和丙烯酸的流动。 除了高质量的成像之外,手术者应当具有足够的知识和专业技能以保证操作的质量和安全性。这些技能包括但并不局限于脊柱和CT以及X线透视上相关结构的放射解剖学的知识,放射物理学的正式培训,对自己和病人暴露最小化的设备和技术的使用,CT或X线透视引导下的脊柱活检程序的操作经验。 最佳的影像引导装置当考虑使用CT和X线透视的双引导(Dual guidance CT and fluoroscopy ) 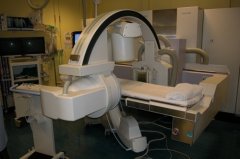 双向数字血管造影设备是理想的椎体成形术引导手段 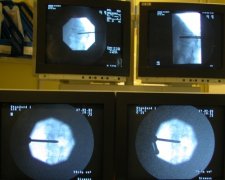 双向数字血管造影设备可以同时观察穿刺针进入椎体的情况,以及骨水泥在椎体内弥漫 最佳的影像引导装置当考虑使用CT和X线透视的双引导(Dual guidance CT and fluoroscopy )
脊椎成形术在操作过程中需要手术者集中注意力,因此,应当有一个专心的护士或者其他受过训练的专业人士,他们的主要任务是建立和维持静脉通道,保持清醒镇痛,监测病人的生理状态和进行医疗记录。对于俯卧位时呼吸幅度减小,导致氧合不足的病人应给与特别的关注。呼吸受累的病人在手术过程中可能需要补充氧气或者麻醉支持。紧急复苏的设备和药物必须马上可用。 在调整俯卧位之前5分钟静脉给一25-50μg的芬太尼(Sublimaze)。骨质疏松病人采用体位复位(postural reduction)方式俯卧在血管造影台上,即俯卧位同时在胸部和盆腔给予支撑,这样的姿势有助于恢复压缩骨折的高度。骨折和后凸脊柱的闭合复位(closed reduction)是利用手术床过伸复位再进行椎体成形术有利于恢复后凸畸形的角度和椎体高度[10]。体位摆好后连接鼻导管给氧和生理监测仪例如EKG导联、脉搏血氧计和血压袖套。另外,根据需要以芬太尼和咪达唑仑(Versed,Roche Pharma)的形式给以清醒镇静。 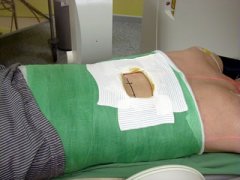 病人俯卧在血管造影台上严格消毒
为了使感染的危险降到最低,操作要在严格的无菌环境中进行。所有工作人员带上手术帽和口罩,手术者需穿上无菌手术服和带无菌手套进行操作。在X线透视下确定病变椎体,标记穿刺水平,备皮,盖上治疗单。增感屏同样用无菌包盖上,因为它处于距离手术者和脊椎成形术设备很近的位置。预防性抗生素治疗,无论是静脉给药或者混合在丙烯酸聚合物中都被提倡。 椎弓根的靶向作用:双椎弓根 vs 单椎弓根路径 向骨折的骨质疏松椎体穿刺,尤其是胸椎的椎体穿刺是通过穿刺椎弓根的途径得以实现的。被穿刺的椎弓根可以在AP(前-后位)的X线透视下被显现出来。X线管球或影像增强器在趋近于椎弓根的过程中,即可以是在前后位,也可以轻微的倾斜。在这个过程中,寻求椎弓根的最大表面积用于靶向定位,此时很容易看到它全部的皮质圆周。 在腰椎经椎弓根途径;在胸椎推荐椎弓根外路径。在椎体骨坏死伴有骨内真空裂隙(intraosseous vacuum clefts)的情况下,如Kummel‘s病,经一侧椎弓根穿刺就可以充盈全部椎体 针的前进定位取决于脊柱注射骨水泥的程度。单侧注射时针尖前进到同侧脊椎体前三分之一的位置。如果需要填充整个脊椎,通常有必要穿刺对侧。使用更加倾斜的(同侧成角20-30度)“Scotty-dog”视角穿刺椎弓根会形成一个从侧面到中间的针迹,最终针的位置接近锥体的中线。从这个位置来看更可能单次椎弓根的注射就可以填充大部分锥体,使对侧穿刺的需要降到最小。这个方法更具有技术挑战性,因为椎弓根的皮质并不能像它在靶心视角中那样可以清楚地显示,并且表面积更小,特别是在胸椎中。如果针定位的太靠外侧,横突可能会骨折或者可能会进入胸腔。无论怎样,上述单一椎弓根的方法需要更短的操作时间,减少了风险,因为仅有一个椎弓根被穿刺,同时获得更好的视野。 使用其他方法应当避免穿刺点位于椎弓根的内侧和下缘。这些位置的示踪剂可以导致破坏皮质层并进入椎管或者神经孔。一旦决定了进针的角度,使用7-10 cc的0.25%盐酸布比卡因,2英寸、25-号的脊髓穿刺针麻醉皮肤、皮下软组织和椎弓根的骨外膜。在拔出针之前,前后位和侧位的X线透视应当显示出针的尖端紧靠椎弓根的位置。如果正侧位的两者之间有偏差,并且病人确实处于侧位,那么前后位的针需要向头侧侧或者尾侧调整直到针的尖端紧靠侧位像中的同样的位置。用11号手术刀片切一个小的皮肤切口制造一个脊椎成形术针的通道。 针的定位 目前有数种被允许在市场销售的骨水泥穿刺针,不同的产品之间的特性大体类似,没有实验能够证实各种不同的针有明显的差异。这些穿刺针通常作为“骨活检”针的型号列成表,大小从11-14G;直径太小的小号针注射骨水泥很困难。骨水泥针考虑的重要特点包括不同针尖形状以及有效长度,针在椎弓根内透视下的可见性,套管中探针的“锁定”以及套管的Luer锁扣座和不同的注射骨水泥的设备及与骨水泥的相容性。介入放射医生应当熟悉各种不同的产品,将它们记在脑子里随时可以调用。在针的定位之后需将进行皮肤浸润麻醉,关于在PVP的操作中的疼痛的处理没有共识,但有研究显示作为单一的麻醉方式,单纯利多卡因的局部麻醉对有些病人是不够充分的[1]。有医生喜欢全麻减少病人的疼痛和紧张。 将针逐渐推进直到探针尖端接触到椎弓根的中点部分的上面的皮质的表面。由于椎弓根的形状不同,针应当进入最宽的点,远离内侧和下缘。侧位像上推进的角度由椎骨压缩的程度或者椎骨前楔程度所决定。进针的过程经常平行于椎骨上面,这种情况下,探针尖端的位置必须在椎弓根的更上方。在前后位像上,针会从外侧到内侧横跨椎弓根和锥体,否则,它会接触或者穿出锥体的外侧壁。 探针尖端必须在破开皮质之前精确地定位。定位最好用钻石头的探针(梅花针头),因为斜面的探针有滑出椎弓根的倾向。一旦开始,重新定位会很困难,因为探针有滑到开始的针痕中的倾向。用轻度来回转动的方式将针尖推入皮质,在这个过程中经常在前后位和侧位平面的X线透视检查来保证针横穿了椎弓根。可以选择使用小的无菌整形外科锤轻轻敲打针柄,使针尖少量地推进。一旦进入到骨小梁中,进针需要更小的力量。同样要小心千万不能穿出终板和椎壁。使用单斜面的探针会允许针尖偏离斜面相反的方向,允许在任何一个平面进行微小的调整。在连续或者间断的侧位X线透视下进针直到探针尖端到达锥体的前三分之一到四分之一之间。尖端在前后位像上距离中线越近,在侧位像上的位置越靠前。因为探针的尖端超过了套管针的末梢,最终套管针的尖端会靠后一点点。 对侧针的位置 许多有经验的介入医生将单个针定位在椎体的中部,仅一侧穿刺就能将骨水泥注射到椎体的中部甚至两侧,也即在一个位置填满整个椎体。如果最初针的位置在半椎体的外侧面之内,骨水泥很有可能留在同侧的半椎体中。当觉得最初的填充不满意或者不完全时会放置第二个针。这对于一个好的临床结果是否有必要是一件可以讨论的事。在Tohmeh等人评价使用单或者双椎弓根注射治疗骨质疏松脊椎的PMMA(聚甲基丙烯酸甲酯)增加物的体外实验显示出在是否增加的组之间压缩性试验的高度改变中没有显著的区别,特别的是,在单边的增加组中没有看到优先的变形。在Kim等人的一个回顾性临床试验中,使用单椎弓根推进在一个穿刺位置填充了两个脊椎半球,这在临床结局上与双椎弓根的脊椎成形术没有显著地统计学差异。 当使用双椎弓根穿刺针推进时,进行一侧注射骨水泥时,对侧的穿刺针的针芯应留在椎体中,否则,骨水泥会穿过对侧针道溢出。在向第二个半椎体注射之前要移出第一根针。另一个可能的问题是在注射过程中椎体中的骨水泥会与针重叠而使针在透视下显得模糊。一个解决方法是在完成第一次注射之后放置第二根针。单针周围的显像可以通过改变侧位的倾斜度很容易完成。另一个技术难题是在对侧注射时由于同侧半椎体中PMMA的存在难以观察骨水泥的流动。可能的解决方法包括在对侧注射时在使用的骨水泥中加入额外的硫酸钡,这样可以透过同侧的骨水泥中看到,使用同侧注射时的最后的图像作为指导寻找溢出到存在的管型之外的骨水泥,或者在结合侧位和前后斜位像之下注射。不建议使用路图技术,因为呼吸和肠道的气体运动不可能得到精确的图像。 脊椎静脉造影术 脊椎静脉造影术最初的想法是在骨水泥注射之前,模拟骨水泥注射作为一个安全性特点提出。在椎体中注射少量的造影剂可以评估丙烯酸外渗的可能的路线以及清楚地定义椎静脉流入前内侧的硬膜外静脉丛的通路。在侧位像上,可以在椎弓根之间的椎体后缘的前面看到像骨性压缩的静脉丛的流出点,这在骨质疏松的骨中是不容易看到的。该血管结合处是很重要的信息,因为丙烯酸外渗到硬膜外静脉是脊椎成形术中神经并发症的主要原因。
在是否需要脊椎造影术存在争议[],特别是在有经验的介入医生手中。Gaughen等人回顾性地评价了在两个病人群体中进行脊椎静脉造影术的安全性和有效性;一组采用而另一组不采用脊椎造影术。结果发现无论静脉外渗的频率或量还是临床结局上,两组之间都没有任何显著差异。该研究是在大的医学中心、由具有广泛经验的资深介入医生操作完成的,该结论可能并不对所有的介入医生都有效。简而言之,一些手术者可能会发现脊椎造影术有帮助,因为它容易鉴别椎体中的硬膜外和椎旁静脉系统的边界以及可以预测PMMA流的特征和可能的流出口。进入主要静脉结构的针的位置的直接检测允许我们可以再次调整其位置,通常是在注射骨水泥之前将针在椎体中再向前推进一些。 因为骨水泥的粘滞性随着时间发生变化,当其呈现牙膏状的时候再注射可以减少骨水泥外溢到周围组织中。 Kallmes 等人证实静脉外溢的程度和频率没有显著的差异,临床结果病人做不做静脉造影没有不同[9]。 骨水泥的准备 尽管在椎体疾病的治疗中已经使用过了种种骨填充物质,聚甲基丙烯酸甲酯(PMMA)是目前美国唯一批准通过的用在脊椎成形术中的生物材料。有好几种商品化的可用于脊椎成形术的PMMA,它们都有不同的操作特点。可注射的丙烯酸由两种成分生成:(1)能或不能放在造影剂中的粉状的聚合物和(2)液态的单体。当这两种物质结合在一起,导致混合物循环递增的聚合反应形成了固体状态。
其具有良好的生物相容性和生物力学强度和硬度。在透视下可视性强和快速固化,在几分钟内立即形成机械稳定性。新的注射物如树脂材料、磷酸钙和硫酸钙,以及新的PMMA制剂已经进入临床应用[11]。高粘稠PMMA系统安全和有效,它可以显著地减少外溢率和减少渗漏导致的并发症[12]。早期结果显示硫酸钙塑形可以通过板层骨(lamellar bone)置换大部分的骨水泥重吸收。但是,部分临床医生已经警告注射可吸收性骨水泥有椎体早期塌陷的危险。Lewis等人报告生物活性的玻璃与PMMA相结合增加轴向强度[13]。生物机械研究显示PMMA约3.5cm大大恢复骨折和邻近椎体正常的应力分布,为了修复运动椎体的硬度和分布在椎体和神经弓(neural arch)之间的负载需要7.5cm[14]。
使用者必须在开始脊椎成形术之前熟悉PMMA。以保证合成的混合物可以被有效地注射到针中并可以在X透视检查中看到的方法。训练骨水泥的使用是很重要的。关于这种物质的文献有很多,特别有意思的是关于不同的PMMA的压缩强度的报告,聚合物中单体和粉剂的比例在强度上的效应和体外丙烯酸固化的温度升高。尽管这些信息很有意思,但没有什么临床意义。
PMMA对于它在脊椎成形术中的使用有重要影响的主要参数是聚合时间和X线下可视性。聚合时间,或者固化率,在不同的产品中不一样,骨水泥膏剂适合注射的时间可能只有5-20分钟。任何PMMA的聚合时间可以通过将粉状的聚合物和液态的单体试剂瓶在使用之前冷藏而延长。为了延长骨水泥的固化时间,需要在注射前将粉状的聚合物成分完全溶解在液态的单体中。否则,在注射的过程中针中的粉剂可能会与单体分离而导致堵塞插管。一些制造商推荐在混合后和注射前要有大概1分钟的溶解时间。
骨水泥有重大意义的第二个参数即是X线下可视性。因为大多数临床相关的并发症是PMMA流到骨外间隙的结果,所以注射过程中材料的X线透视检查图像是最重要的。图像受到产品中硫酸钡含量,病人的体型,所治疗椎体的位置以及成像系统的质量的影响。因此所有脊椎成形术的放射介入医生必须熟悉它们所选择的PMMA的X线下可视性特性并准备好在需要的时候往混合物中添加额外的硫酸钡。脊椎成形术中使用的无菌的硫酸钡已经商品化了,任何添加的材料应当在膏剂准备之前与粉剂聚合物完全混合以保证均匀混合化。预防注射用的抗生素粉剂,例如妥布拉霉素或者万古霉素也可以加到粉剂聚合物中。制造商的产品和物质添加中的混合说明书的任何改变以及粉剂和液体的比例的变化都会改变材料的粘度和聚合时间。严格地讲,改变的材料不会再被FDA审批通过。
骨水泥的注射
在透视引导下(最好是双向透视)骨水泥的注射应该缓慢进行,操作者要保持高度的注意力观察骨水泥在椎体内弥散的情况,在没有球囊扩张的情况下骨水泥的弥散有时不是均匀分布的。一旦发生骨水泥外溢立即停止操作,此时比较困难的是残余在穿刺针内的骨水泥,如果用针栓推出残余的骨水泥势必加重骨水泥外溢的情况,如果拔针,穿刺针内的骨水泥会残留到针道内会造成病人在仰卧时的不适感。最好的办法是提前预估骨水泥外溢的可能性,在发现外溢之前停止注射骨水泥。特别是前2/3椎体已经被骨水泥充盈,在上下两个椎间盘均匀分布的时候。一项研究显示骨水泥充盈或骨水泥渗漏与疼痛缓解之间没有关系[3]。一般骨水泥2.5~12ml可以是骨折椎体充分充盈并达到止痛的目的。Lee 等人特殊设计的螺旋注射器可以使医生精确稳定地注射骨水泥[5]。
1. A. Venmans, C.A. Klazen, P.N. Lohle and W.J. van Rooij Percutaneous Vertebroplasty and Procedural Pain American Journal of Neuroradiology Published January 6, 2010 2. Laredo JD, Hamze B. Complications of percutaneous vertebroplasty and their prevention. Skeletal Radiol 2004;33:493-505. 3. Mousavi P, Roth S, Finkelstein J, Cheung G, Whyne C. Volumetric quantification of cement leakage following percutaneous vertebroplasty in metastatic and osteoporotic vertebrae. J Neurosurg 2003;99:56-9. 4. Chen JF, Lee ST, Lui TN, Wu CT, Liao CC. Percutaneous vertebroplasty for the treatment of osteoporotic vertebral compression fractures: a preliminary report. Chang Gung Med J 2002;25:306-14. 5. Lee ST, Chen JF. A syringe compressor for vertebroplasty: technical note. Surg Neurol 2004;61:580-4. 6. Deramond H, Depriester C, Galibert P, Le Gars D. Percutaneous vertebroplasty with polymethylmethacrylate. Technique, indications, and results. Radiol Clin North Am 1998;36:533-46. 7. Mathis JM. Percutaneous vertebroplasty: complication avoidance and technique optimization. AJNR Am J Neuroradiol 2003;24:1697-706. 8. Vasconcelos C, Gailloud P, Beauchamp NJ, Heck DV, Murp hy KJ. Is percutaneous vertebroplasty without pretreatment venography safe? Evaluation of 205 consecutives procedures. AJNR Am J Neuroradiol 2002;23:913-7. 9. Chen LH, Lai PL, Chen WJ. Unipedicle percutaneous vertebroplasty for spinal intraosseous vacuum cleft. Clin l Orthop Relat Res 2005;435:148-53. 10. Lee ST, Chen JF. Closed reduction vertebroplasty for the treatment of osteoporotic vertebral compression fractures. Technical note. J Neurosurg 2004;100:392-6. 11. Lieberman IH, Togawa D, Kayanja MM. Vertebroplasty and kyphoplasty: filler materials. Spine J 2005;5:305S-316S. 12. Anselmetti GC, Zoarski G, Manca A, Masala S, Eminefendic H, Russo F, Regge D. Percutaneous vertebroplasty and bone cement leakage: clinical experience with a new high-viscosity bone cement and delivery system for vertebral augmentation in benign and malignant compression fractures. Cardiovasc Intervent Radiol 2008;31:937-47. 13. Lewis G, Towler MR, Boyd D, German MJ, Wren AW, Clarkin OM, Yates A. Evaluation of two novel aluminumfree, zinc-based glass polyalkenoate cements as alternatives 14. Luo J, Daines L, Charalambous A, Adams MA, Annesley-Williams DJ, Dolan P. Vertebroplasty: only small cement volumes are required to normalize stress distributions on the vertebral bodies. Spine 2009;34:2865-73. |